당뇨병성 케톤산증
당뇨병성 케톤산증(영어: diabetic ketoacidosis, DKA)은 당뇨병의 합병증으로 나타나는 케톤산증으로서, 생명을 위협할 수 있는 질병이다.[1] 나타나는 증상과 징후로는 구토, 복통, 쿠스마울호흡, 다뇨, 쇠약, 혼란, 혼수 등이 있다.[1] 또한 날숨에서 특이한 과일향이 날 수 있다.[1] 증상은 대개 빠르게 나타난다.[1] 이전에 당뇨병으로 진단 받지 않은 사람도 당뇨병성 케톤산증이 당뇨병의 첫 신호로 나타날 수 있다.[1]
 | |
|---|---|
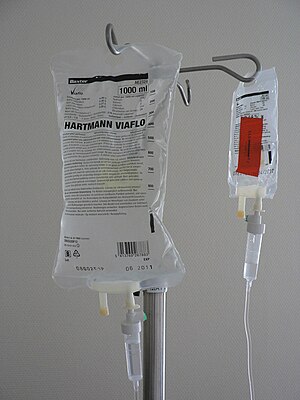 | |
| 당뇨병성 케톤산증에서는 심한 탈수가 생길 수 있어 치료 중 정맥으로 수액을 투여하여야 한다. | |
| 진료과 | 내분비내과 |
| 증상 | 구토, 복통, 깊고 빠른 호흡, 다뇨, 혼란, 특이한 입냄새[1] |
| 합병증 | 뇌부종[2] |
| 통상적 발병 시기 | 비교적 빠름[1] |
| 병인 | 인슐린 부족[3] |
| 위험 인자 | 보통 제1형 당뇨병에서 발병, 그 외의 당뇨병에서는 비교적 덜 발병[1] |
| 진단 방식 | 고혈당, 산증, 케톤산[1] |
| 유사 질병 | 고삼투압성 고혈당 증후군, 알코올성 케톤산증, 요독증, 살리실산염 중독[4] |
| 치료 | 수액, 인슐린, 칼륨[1] |
| 빈도 | 연간 제1형 당뇨병 환자의 4 ~ 25%[1][5] |
제1형 당뇨병 환자에서 당뇨병성 케톤산증이 가장 자주 발병하지만 특정 상황에서는 다른 종류의 당뇨병 환자에게도 당뇨병성 케톤산증이 발생할 수 있다. 발병의 촉발 요인으로는 감염, 인슐린 투여를 놓친 경우, 스테로이드와 같은 약물의 투약 오류 등이 있다.[1] 당뇨병성 케톤산증은 인슐린이 부족해져 신체가 지방산을 연료로 사용하고 그 결과 산성을 띠는 케톤체가 만들어지기 때문에 발생한다.[3] 고혈당, 산증, 혈액이나 소변 내의 케톤산을 발견했을 때 당뇨병성 케톤산증으로 진단할 수 있다.[1]
당뇨병성 케톤산증의 일차 치료는 수액과 인슐린 투여이다.[1] 중증도에 따라 인슐린을 정맥 주사하거나 피하 투여한다.[3] 보통 저칼륨혈증의 발생을 예방하기 위해 칼륨도 함께 투여하여야 한다.[1] 치료 도중 혈당과 칼륨 수치를 주기적으로 확인하여야 한다.[1] 당뇨병성 케톤산증의 기저 원인 역시 확인할 필요가 있다.[6] 혈중 pH가 매우 낮고 상태가 위독한 환자에게는 탄산수소 나트륨을 투여할 수도 있으나, 그 효과는 불분명하므로 일반적으로는 권고되지 않는다.[1][6]
당뇨병성 케톤산증의 발병률은 국가마다 다르다.[5] 매년 영국에서는 제1형 당뇨병 환자의 4%가 당뇨병성 케토산증에 걸리는 반면, 말레이시아에서는 환자 100명 가운데 26.3명 꼴로 당뇨병성 케톤산증이 발병한다.[1][5] 당뇨병성 케톤산증은 1886년에 처음 기술되었으며, 1920년대에 인슐린 치료가 도입되기 전까지는 거의 항상 치명적이었다.[7] 적절한 치료를 제때 시행한다면 사망률은 1 ~ 5% 정도이다.[1][6]
증상 및 징후 편집
당뇨병성 케톤산증의 증상은 24시간 정도에 걸쳐 발생한다. 주된 증상으로는 구역질과 구토, 확연한 갈증, 소변량이 늘어나는 다뇨, 심각하게 나타나기도 하는 복통 등이 있다. 중증의 당뇨병성 케톤산증에서는 빠르고 헐떡이는 듯하며 깊은 양상의 호흡이 나타나는데 이를 쿠스마울호흡이라고 한다.[8][9] 복부에서는 급성 췌장염, 맹장염, 위장관 천공 등의 심각한 복부 질환이 의심될 정도로 압통이 느껴질 수 있다.[9] 적은 수의 사람에서는 커피찌꺼기모양 구토가 나타나기도 하며 식도의 미란에서 발생하는 경향이 있다.[7] 심각한 당뇨병성 케톤산증에서는 환자가 혼란을 겪거나 의식수준이 저하되며 혼수 상태에 빠지기도 한다.[6][9]
신체검사에서는 보통 입이 말라 있거나 피부 긴장도가 줄어들어 있는 등 탈수의 임상적 증거가 보인다. 탈수가 순환 혈액량을 감소시킬 정도로 심하다면 심박수가 빨라지는 빈맥과 혈압이 감소하는 저혈압을 확인할 수도 있다. 종종 케톤산으로 인해 날숨에서 과일향이나 배 드롭 냄새가 날 수도 있다고 묘사된다.[1][9] 이러한 냄새는 환자의 날숨에 존재하는 아세톤 때문이다.[10] 쿠스마울호흡이 있다면 호흡수가 증가하는 빈호흡으로 나타난다.[9]
당뇨병성 케톤산증이 있는 소아는 뇌부종에 비교적 취약해지며, 이로 인해 두통, 혼수, 동공반사 소실이 유발될 수 있고 사망에까지 이를 수 있다. 뇌부종은 당뇨병성 케톤산증 환아의 1% 정도에서 발생하며 성인에서는 더 드물다.[3][9][11]
원인 편집
당뇨병성 케톤산증은 본인이 당뇨병이 있다는 것을 아는 사람들에게 가장 흔히 발생하지만, 이전까지 당뇨병이 있다는 것을 몰랐던 사람들에서 첫 증상으로 나타날 수도 있다. 당뇨병성 케톤산증으로 이어지기도 하는 특정 기저 원인들이 있는데 이러한 원인에는 병발성 질환(폐렴, 독감, 위장관염, 요로감염증), 임신, 불충분한 인슐린 투여(인슐린 펜이 고장난 경우 등), 심근경색, 뇌졸중, 코카인 복용 등이 있다. 젊은 환자들의 경우 기저질환으로 식사장애를 가지고 있거나, 체중이 증가할 것을 걱정해 인슐린을 불충분하게 사용하면 당뇨병성 케톤산증이 재발할 수 있다.[9]
이전에 제2형 당뇨병이 있다고 밝혀진 사람이나, 추가 조사에서 제2형 당뇨병의 특징(비만, 강한 가족력 등)이 있는 것으로 밝혀진 사람에서 당뇨병성 케톤산증이 발생할 수도 있다. 이는 아프리카인, 아프리카계 미국인, 히스패닉에서 더 흔하다. 이러한 상태를 '케톤증 경향 제2형 당뇨병'(ketosis-prone type 2 diabetes)으로 분류한다.[3][12]
제2형 당뇨병에 일반적으로 사용하는 SGLT2 억제제 클래스에 속하는 약물들은 혈당 수치가 크게 올라가지 않는 당뇨병성 케톤산증(정상혈당성 DKA, euglycemic DKA) 발생과 관련이 있다고 알려져 있다.[13] SGLT2 억제제 투여로 인한 당뇨병성 케톤산증은 비교적 흔치 않은 부작용이지만, 만약 SGLT2 억제제와 인슐린을 동시에 사용 중인 환자가 인슐린 투여를 놓치거나 투여량을 줄일 경우 더 흔하게 발생한다고 여겨진다. 또한 중증의 급성 질환, 탈수, 고강도의 운동, 수술, 저탄수화물 식이요법, 과도한 알코올 섭취에 의해 당뇨병성 케톤산증이 촉발될 수 있다.[13] 혈량저하증과 상대적 인슐린 결핍, 글루카곤 증가 등으로 인해 케톤증이 생긴다는 설명이 SGLT2 억제제로 인한 정상혈당 DKA의 기전으로 제안되기도 했다.[14] 수술 전에는 SGLT2 억제제 투여를 멈추고 안전하다고 판단될 때 투여를 재개해야 한다.[15] SGLT2 억제제는 제1형 당뇨병 환자에서도 쓰일 수 있으나, 케톤산증의 가능성이 있으므로 특별한 위험 관리가 필요하다. 특히 저탄수화물이나 케톤생성 식이요법을 하고 있는 사람에게는 SGLT2 억제제를 쓰지 말아야 한다.[16]
발병 기전 편집
당뇨병성 케톤산증은 체내 인슐린의 작용이 부족하여 발생한다. 인슐린의 작용이 감소하고 그에 따라 글루카곤이 증가하면 간의 포도당신생과 글리코겐으로부터의 포도당 방출이 증가한다. 정상적으로 이 과정은 인슐린에 의해 억제된다. 많아진 포도당은 물과 나트륨, 칼륨 등의 용질과 함께 소변으로 배설되는데 이 과정을 삼투성 이뇨라고 한다.[3] 삼투성 이뇨로 인해 다뇨, 탈수, 다음증이 증상으로 나타난다. 또한 인슐린 부족은 지방조직에서 자유 지방산이 방출되도록 지방분해를 일으킨다. 이때 간에서는 자유 지방산을 베타 산화시켜 아세틸 CoA로 만든다. 아세틸 CoA는 굶었을 때와 같이 심각한 에너지 결핍 상태인 경우 케톤생성 과정을 통해 케톤체로 대사된다. 케톤생성 과정의 최종 산물은 아세토아세테이트와 베타-하이드록시뷰티레이트이다. 인슐린을 통한 포도당 전달이 되지 않을 때 이 두 케톤체는 에너지원으로서의 역할을 할 수 있으며, 굶었을 때 에너지를 공급하기도 한다. 그러나 케톤체는 pKa가 낮으므로 혈액을 산성으로 만들며 대사성 산증을 일으킨다. 처음에는 신체가 이에 대응하여 중탄산염 완충계를 통해 산성으로의 변화를 완충하지만, 중탄산염 완충계는 빠르게 산증에 의해 압도되므로 산증을 보상하기 위해 다른 기전들이 작동해야 한다.[3] 그러한 기전들 중 하나는 혈중 이산화탄소를 낮추기 위한 과호흡(호흡보상)이다. 과호흡이 심해지면 쿠스마울호흡의 양상으로 나타난다.[9]
감염과 같은 여러 상황에서 인슐린 필요량은 증가하지만 이자의 생산량은 그 필요량을 만족하지 못한다.따라서 혈당 수치가 올라가며 뒤이어 탈수가 오고, 악순환이 반복되며 인슐린 저항성이 증가한다.[3][7]
위의 기전에 의해 당뇨병성 케톤산증이 있는 성인은 평균적으로 6L (또는 100mL/kg)의 수분이 부족해지며 나트륨, 칼륨, 인, 마그네슘, 칼슘 등도 감소한다. 혈당 수치는 보통 13.8mmol/L 또는 250 mg/dL을 넘는다.[17]
당뇨병성 케톤산증은 제1형 당뇨병에서 흔한데, 이는 제1형 당뇨병은 랑게르한스섬에서 생산하는 인슐린이 절대적으로 부족해지면서 발병하기 때문이다. 제2형 당뇨병에서는 인슐린 생산이 이루어지지만 말초 기관에서의 인슐린 저항성으로 인해 인슐린 생산량이 체내 필요량을 충족하지 못한다. 보통 제2형 당뇨병의 인슐린 생산량은 케톤생성을 억제할 정도로는 충분하다. 제2형 당뇨병 환자에서 당뇨병성 케톤산증이 발생한 경우 케톤증 경향 제2형 당뇨병이라고 한다.[12] 이러한 현상의 정확한 기전은 불명이나 인슐린 분비의 손상과 작용 과정 손상에 대해 모두 근거가 있다.[3][12] 당뇨병성 케톤산증을 치료하면 인슐린 생산이 재개되며 종종 제2형 당뇨병에서 보통 권고하는 치료법도 다시 시작할 수 있다.[3]
당뇨병성 케톤산증의 임상적 상태에는 위의 발병 기전과 더불어 글루카곤과 아드레날린 등의 여러 길항호르몬과 사이토카인이 관련되어 있다. 사이토카인은 염증의 표지자로, 감염이 없더라도 증가할 수 있다.[3][18]
당뇨병성 케톤산증의 가장 위험한 합병증인 뇌부종은 여러 가지 요인으로 인해 발생한다고 여겨진다. 일각에서는 뇌부종이 지나치게 많은 수액 보충으로 인한 것이라고 주장하지만, 치료가 시행되기 전부터 뇌부종이 생기기도 한다.[11][19] 중증 당뇨병성 케톤산증인 경우[18]와 처음으로 당뇨병성 케톤산증이 발생한 경우 뇌부종의 위험이 더 높다.[11] 뇌부종 발생의 가능성이 있는 요인에는 탈수, 산증, 낮은 혈중 이산화탄소 농도가 있다. 그 외에도 염증과 혈액응고가 증가하면 앞의 요인들과 함께 뇌의 일부로 가는 혈액량을 감소시켜 수액 투여가 시작됐을 때 뇌부종을 유발할 수 있다.[11] 뇌 조직의 부종은 머리속압력을 증가시켜 궁극적으로는 사망에 이르게 한다.[18][19]
진단 편집
조사 편집
고혈당증, 혈액이나 소변의 케톤, 산증이 함께 있을 때 당뇨병성 케톤산증으로 진단할 수 있다.[6] 10%의 환자는 혈당이 크게 올라가지 않는 정상혈당성 케톤산증의 양상을 보인다.[3]
산증을 확인하기 위해 pH를 측정한다. 동맥과 정맥의 혈액 pH는 거의 차이가 없으므로 정맥의 혈액으로도 pH를 측정하는 데에는 충분하다. 산소 농도에 대한 검사가 필요할 때만 동맥혈 표본이 필요하다.[6] 케톤을 측정하기 위해 소변에서 아세토아세테이트를, 혈액에서 베타-하이드록시뷰티레이트를 측정한다. 소변 아세토아세테이트 검사와 비교했을 때, 모세혈관 혈액의 베타-하이드록뷰티레이트 측정은 입원의 필요성을 줄이며, 입원을 했을 때 그 기간을 줄이며 환자의 병원 비용을 줄일 수 있다.[20] 케톤 농도가 매우 높다면 모세혈관 혈액에서의 케톤 측정이 부정확해질 수 있다.[21]
위의 검사들에 더해 보통 요소, 크레아티닌, 전해질 농도를 측정하기 위해 혈액 표본을 얻는다. 요소와 크레아티닌은 당뇨병성 케톤산증 환자에서 손상될 수 있는 콩팥기능을 검사하기 위해 측정한다. 또한 감염 표지자인 일반 혈액 검사와 C반응단백(CRP), 급성 췌장염의 표지자인 아밀레이스와 라이페이스도 측정할 수 있다. 감염을 배제하기 위해 흉부 X선과 소변검사를 흔히 시행한다.[3]
혼란, 재발성 구토, 기타 다른 증상 때문에 뇌부종이 의심된다면 그 중증도를 평가하고 뇌졸중과 같은 다른 원인을 배제하기 위해 CT를 시행할 수 있다.[19]
기준 편집
당뇨병성 케톤산증은 혈액과 소변에 존재하는 다량의 케톤, 심각한 대사성 산증을 통해 다른 당뇨병성 응급질환과 감별할 수 있다. 제2형 당뇨병에서는 당뇨병성 케톤산증보다 고삼투압성 고혈당 증후군(HHS)이 훨씬 흔한데, 고삼투압성 고혈당 증후군에서는 심각한 탈수로 인해 혈장 삼투압농도가 320mosm/kg 이상으로 증가한다. 가벼운 산증과 케톤혈증이 나타나기도 하지만 당뇨병성 케톤산증만큼 심하게 나타나지는 않는다. 당뇨병성 케톤산증에서도 삼투압농도가 증가할 수 있으므로 두 질환 사이에는 어느 정도 겹치는 부분이 있다.[3]
케톤산증은 당뇨병으로 인해서만 발생하지는 않는다. 알코올 의존증이나 폭음에 의한 알코올성 케톤산증, 심하게 굶어서 발생하는 기아성 케톤산증도 있다. 두 경우에서 모두 혈당 수치는 정상이거나 낮다. 당뇨병 환자에서 에틸렌 글라이콜이나 파라알데하이드 등에 의한 중독과 같은 다른 이유로 대사성 산증이 나타나기도 한다.[3]
미국당뇨협회에서는 성인의 당뇨병성 케톤산증을 중증도에 따라 세 개의 병기로 나눈다.[3]
- 경도: 혈중 pH가 7.25에서 7.30 사이로 약간 떨어져 있다. (정상 pH는 7.35 ~ 7.45) 혈청 중탄산염 농도는 15 ~ 18mmol/L로 떨어져 있다. (정상 중탄산염 농도는 20mmol/L 이상) 환자의 의식은 명료하다.
- 중등도: 혈중 pH 7.00 ~ 7.25, 중탄산염 농도 10–15mmol/L, 환자는 약간 졸려 할 수 있다.
- 중증: 혈중 pH 7.00 이하, 중탄산염 농도 10mmol/L 이하, 환자가 혼미나 혼수 상태에 빠질 수 있다.
유럽소아내분비학회(European Society for Paediatric Endocrinology)와 로슨 윌킨스 소아내분비학회(Lawson Wilkins Pediatric Endocrine Society)의 2004년 기준은 소아에 대해서 약간 다른 기준값을 사용하고 있다. 경도 당뇨병성 케톤산증은 pH 7.20 ~ 7.30(중탄산염 농도 10 ~ 15mmol/L), 중등도는 pH 7.10 ~ 7.20(중탄산염 농도 5 ~ 10mmol/L), 중증은 pH 7.1 미만(중탄산염 농도 5mmol/L 미만)으로 정의하고 있다.[18]
예방 편집
당뇨병 환자는 일정한 규칙('sick day rules')을 준수하여 당뇨병성 케톤산증 발작을 어느 정도 예방할 수 있다.[6] 이 규칙은 환자가 몸이 좋지 않을 때 어떻게 자기 자신을 치료할 수 있는지에 대한 명확한 지침이다. 지침에는 혈당 수치가 조절되지 않을 때 얼마만큼의 인슐린을 추가로 투여해야 하는지에 관한 조언과, 소금과 탄수화물이 풍부하면서 쉽게 소화가 되는 식단, 발열을 억제하고 감염을 치료하는 방법, 의학적인 도움을 요청할 때의 권장 사항 등이 포함되어 있다.[3]
또한 당뇨병 환자는 몸이 좋지 않을 때 자신의 케톤 농도를 지켜보고 만일 케톤 농도가 올라갔다면 도움을 요청할 수 있다.[22]
치료 편집
당뇨병성 케톤산증 치료의 주된 목표는 체내에서 손실된 체액과 전해질을 보충하면서 인슐린을 통해 고혈당과 케톤 생산은 억제하는 것이다. 집중치료실(ICU)과 준중환자실(HDU)로 보내 면밀하게 관찰해야 할 수 있다.[6]
체액 보충 편집
추정되는 탈수의 정도에 따라 보충하는 수액의 양이 달라진다. 혈압이 심하게 떨어지며 신체 기관에 혈액이 충분히 공급되지 못하는 쇼크 상태에 이를 정도로 탈수가 심각하거나 의식이 저하되는 경우, 식염수를 성인에게는 1L, 소아에게는 10mL/kg을 빠르게 반복 투여하여 순환 혈액량을 회복하도록 권고한다.[3][23] 탈수가 중등도라면 수분과 나트륨이 얼마나 부족한지 계산하여 더 느리게 수액을 보충할 수 있으며 이때도 식염수를 수액으로 권장한다.[22][23] 구토가 없는 매우 경도의 케톤산증과 경도의 탈수는 악화 소견이 나타나는지 관찰하면서 인슐린 정맥 주사 없이 경구나 피하 수액으로 치료할 수 있다.[23]
대개 생리식염수(0.9% NaCl)가 수액으로 쓰인다.[24] 거의 차이가 없는 다른 균형 잡힌 수액에 대한 몇몇 작은 임상시험이 있었다.[24]
특이하지만 흔치 않은 고려 질환에는 탈수가 아닌 심장의 혈액을 혈관으로 펌프질하는 능력이 약해져 혈압이 떨어지는 심장성 쇼크가 있다. 이 경우 집중치료실로 환자를 옮긴 뒤 상반신의 큰 정맥에 중심정맥관을 삽입하여 중심정맥압을 감시하며, 심장의 펌프 기능과 혈압을 증가시키는 약물인 수축촉진약을 투여한다.[3]
인슐린 편집
몇몇 가이드라인에서는 인슐린을 kg당 0.1U로 일시주사할 것을 권고한다. 이때 칼륨 농도가 3.3mmol/L보다 높아진 직후 인슐린을 일시주사한다. 만일 칼륨이 그보다 낮은 경우에 인슐린을 투여하면 칼륨이 위험한 수준까지 떨어질 수 있다.[3] 다른 가이드라인에서는 인슐린 정맥 주사가 지연되는 경우 근육 주사로 일시에 인슐린을 투여할 것을 권고하나,[6] 소아를 대상으로 한 가이드라인에서는 수액 투여 전까지 인슐린 투여를 연기하라고 권장한다.[23] 경도나 중등도인 경우 속효성 인슐린 유사체를 피하 주사할 수도 있다.[25]
일반적으로 혈당을 줄이고 케톤 생산을 억제하기 위해 시간당 0.1U/kg의 인슐린을 투여한다. 혈당 수치가 떨어지기 시작할 때의 인슐린 투여량은 가이드라인에 따라 다르다. 미국의 가이드라인에서는 혈당이 16.6mmol/L (300mg/L) 이하로 떨어질 때 인슐린 투여량을 줄이라고 권고한다.[3] 영국의 가이드라인은 14mmol/L (253mg/dL)를 기준으로 한다.[6] 다른 가이드라인에서는 고용량의 인슐린 투여를 유지하기 위해 식염수에 포도당를 추가하여 투여하라고 권장한다.[22][23]
칼륨 편집
칼륨 농도는 당뇨병성 케톤산증 치료 중에 심하게 변화할 수 있는데, 이는 인슐린이 나트륨-칼륨 펌프의 활성을 증가시켜 칼륨이 세포 안으로 들어가게 해 혈중 칼륨 농도를 감소시키기 때문이다. 이동된 세포외 칼륨의 대부분은 삼투성 이뇨 때문에 소변으로 손실된다. 치료 이후 저칼륨혈증이 발생하기도 하며, 이는 부정맥의 위험을 높인다. 따라서 심박수를 지속적으로 관찰하는 것이 권장되며,[6][23] 칼륨 농도를 반복적으로 측정해야 한다. 또한 칼륨이 5.3mmol/L 이하로 떨어진다면 수액에 칼륨을 추가한다. 칼륨이 3.3mmol/L 이하로 떨어지면 저칼륨혈증을 교정하기 위해 인슐린 투여를 멈춰야 할 수도 있다.[3]
탄산수소 나트륨 편집
산증을 빠르게 개선하기 위한 탄산수소 나트륨 용액 투여에는 논란이 있다. 실제로 표준 치료에 비해 결과가 개선된다는 근거는 거의 없고 산증을 개선할 수도 있다는 근거는 약간 있으나, 세포 내부의 산증은 악화시킬 수 있으며 특정 합병증의 위험도 증가시킬 수 있다. 따라서 일반적으로 탄산수소 나트륨 사용은 권장되지 않는다.[6][18][22] 다만 몇몇 가이드라인에서는 극심한 산증(pH < 6.9)에 대해, 소수의 가이드라인에서는 중증 산증(pH 6.9 ~ 7.0)에 대해 사용을 권장하기도 한다.[3]
뇌부종 편집
뇌부종이 혼수와 함께 나타난 경우 반드시 집중치료실로 옮기고 기계환기를 시행하며 면밀히 관찰해야 하는 경우가 자주 있다. 수액 투여는 느리게 시행한다. 당뇨병성 케톤산증에서 뇌부종의 이상적인 치료법은 아직 제대로 수립되지 않았으나, 부종을 줄이기 위해 다른 일부 뇌부종에서 시행하기도 하듯이 정맥으로 만니톨과 고장성 식염수(3% NaCl)를 주입한다.[18] 뇌부종은 성인에서는 드물다.[6]
해소 편집
당뇨병성 케톤산증의 해소는 증상의 전반적인 개선, 즉 경구로 영양과 수액을 섭취할 수 있으며, 체내 pH가 7.3보다 높아졌으며, 혈액(1mmol/L 미만)이나 소변에 케톤이 없는 상태로 정의된다. 이 상태에 한번 도달하면 인슐린을 피하 주사 요법으로 전환하고, 정맥 주사는 이로부터 1시간 뒤에 중단한다.[6][23]
케톤증 경향 제2형 당뇨병 환자에서는 글루탐산 탈탄산효소와 랑게르한스섬 세포에 대한 항체 여부를 확인하는 것이 인슐린 투여를 장기적으로 계속할지 결정하는 데에 도움이 될 수 있다. 항체가 검출된 경우 장기 투여를 계속하고, 검출되지 않았다면 보통의 제2형 당뇨병처럼 인슐린 투여를 중지하고 경구 약물로 치료를 시도할 수 있다.[12] 일반적으로 환자가 제1형 당뇨병이나 제2형 당뇨병이라고 실제로 의심되지 않는 한 인슐린 생산의 척도로서 C-펩타이드를 일상적으로 측정하는 것은 권장되지 않는다.[22]
역학 편집
당뇨병 환자 1000명당 4.6 ~ 8.0명 정도에서 당뇨병성 케톤산증이 매년 발병한다.[17] 제1형 당뇨병 환자에서의 연간 당뇨병성 케톤산증 발생률은 이보다 높아, 영국에서는 약 4%이며 말레이시아에서는 약 25%이다.[1][5] 미국의 경우 당뇨병성 케톤산증으로 인해 매년 135,000명이 입원하며 이로 인한 추정 비용은 24억 달러에 이른다. 이는 제1형 당뇨병 치료를 받고 있는 환자들이 치르는 총 비용의 25%에서 50% 정도이다. 또한 당뇨병성 케톤산증으로 인해 입원하는 경향이 갈수록 늘고 있다고 기록되어 있다.[3] 식사장애나 인슐린 비용을 부담할 수 없는 등 현재진행형의 위험 인자가 있는 경우 당뇨병성 케톤산증 발생 위험이 증가한다.[3] 제1형 당뇨병 환아의 30%는 당뇨병성 케톤산증을 한번 겪은 뒤에 당뇨병으로 진단을 받는다.[26] 한편 사회경제적 지위가 낮고 거주 지역이 가난할수록 제1형 당뇨병 환자에서의 당뇨병성 케톤산증 발생 위험이 올라간다.[27]
이전에는 항상 치명적이라고 생각되었으나, 적절하게 제때 치료하면 사망 위험은 1 ~ 5%이다.[1][6] 당뇨병성 케톤산증 환아의 뇌부종 발생 위험은 1% 정도이다.[2] 미국에서 당뇨병성 케톤산증 환아의 뇌부종 발생률은 2002년 0.4%에서 2012년에는 0.7%로 증가하였다.[28] 뇌부종이 발생한 환아의 10명 중 2명에서 5명 정도는 뇌부종으로 인해 사망한다.[19]
역사 편집
최초로 당뇨병성 케톤산증을 완전히 설명한 것은 영국 맨체스터에서 일하던 독일의 병리학자인 율리우스 드레슈펠트(Julius Dreschfeld)이다. 그는 1886년 런던의 영국 왕립의사회에서 아돌프 쿠스마울(Adolph Kussmaul)의 보고서를 바탕으로 케톤산증의 주된 케톤인 아세토아세테이트와 베타-하이드록시뷰티레이트에 대해 설명하는 강의를 진행했다.[29] 1920년대에 인슐린이 발견되기 전까지 당뇨병성 케톤산증은 거의 항상 치명적인 질환이었다. 1930년대에 들어서 사망률은 29%까지 떨어졌으며,[7] 1950년대에는 10% 밑으로 감소하였다.[30] 당뇨병성 케톤산증으로 인한 뇌부종의 실체는 필라델피아의 의사 팀에 의해 1936년 기술되었다.[19][31]
1950년대 이후로 이루어진 수많은 연구는 당뇨병성 케톤산증의 이상적인 치료법에 초점을 두었다. 이 연구들의 상당수는 테네시 헬스사이언스센터 대학교와 에모리 의과대학에서 수행했다.[30] 연구되었던 치료 선택지로는 고용량 또는 저용량의 인슐린을 정맥 주사, 피하 주사, 근육 주사하는 요법, 인 보충, 인슐린 부하용량의 필요성, 중등도 당뇨병성 케톤산증에서 중탄산염 치료의 적절성 등이 있다.[30] 그러나 아직 밝혀지지 않은 여러 가지 의문들이 있는데 그 예시로는 중증 당뇨병성 케톤산증에서 중탄산염 치료가 임상적 경과에 실질적인 차이를 만들어내는지, 또는 성인에서 인슐린 부하용량이 필요한지에 관한 의문이 있다.[30]
케톤증 경향 제2형 당뇨병의 실체는 여러 가지 선행 증례 보고 이후 1987년에 완전히 설명되었다. 처음에는 단일유전자 당뇨병의 일종으로 생각되었으며,[32] '케톤증 경향 제2형 당뇨병'(ketosis-prone type 2 diabetes)이라는 용어가 현대에 채택되기 전까지는 '특발성 제1형 당뇨병'(idiopathic type 1 diabetes), '플랫부쉬 당뇨병'(Flatbush diabetes), '비정형 당뇨병'(atypical diabetes), '제1.5형 당뇨병'(type 1.5 diabetes) 등의 여러 이름으로 불려왔다.[3][12]
참고 문헌 편집
- ↑ 가 나 다 라 마 바 사 아 자 차 카 타 파 하 거 너 더 러 머 버 서 어 Misra S, Oliver NS (October 2015). “Diabetic ketoacidosis in adults”. 《BMJ》 351: h5660. doi:10.1136/bmj.h5660. hdl:10044/1/41091. PMID 26510442. S2CID 38872958.
- ↑ 가 나 Bialo SR, Agrawal S, Boney CM, Quintos JB (February 2015). “Rare complications of pediatric diabetic ketoacidosis”. 《World Journal of Diabetes》 6 (1): 167–174. doi:10.4239/wjd.v6.i1.167. PMC 4317308. PMID 25685287.
- ↑ 가 나 다 라 마 바 사 아 자 차 카 타 파 하 거 너 더 러 머 버 서 어 저 처 커 터 Kitabchi AE, Umpierrez GE, Miles JM, Fisher JN (July 2009). “Hyperglycemic crises in adult patients with diabetes”. 《Diabetes Care》 32 (7): 1335–1343. doi:10.2337/dc09-9032. PMC 2699725. PMID 19564476.
- ↑ Ferri FF (2010). 《Ferri's Differential Diagnosis: A Practical Guide to the Differential Diagnosis of Symptoms, Signs, and Clinical Disorders》 (영어). Elsevier Health Sciences. 146쪽. ISBN 978-0323076999. 2017년 9월 8일에 원본 문서에서 보존된 문서.
- ↑ 가 나 다 라 Maletkovic J, Drexler A (December 2013). “Diabetic ketoacidosis and hyperglycemic hyperosmolar state”. 《Endocrinology and Metabolism Clinics of North America》 42 (4): 677–695. doi:10.1016/j.ecl.2013.07.001. PMID 24286946.
- ↑ 가 나 다 라 마 바 사 아 자 차 카 타 파 하 거 Joint British Diabetes Societies Inpatient Care Group (June 2021). “The Management of Diabetic Ketoacidosis in Adults”. Association of British Clinical Diabetologists. 2021년 12월 9일에 원본 문서에서 보존된 문서. 2021년 8월 10일에 확인함.
- ↑ 가 나 다 라 Eledrisi MS, Alshanti MS, Shah MF, Brolosy B, Jaha N (May 2006). “Overview of the diagnosis and management of diabetic ketoacidosis”. 《The American Journal of the Medical Sciences》 331 (5): 243–251. doi:10.1097/00000441-200605000-00002. PMID 16702793.
- ↑ Marcdante KJ, Kliegman R (2015). 〈Diabetes Melitus〉. Marcdante KJ, Kliegman R, Nelson WD. 《Nelson Essentials of Pediatrics》 7판. 573–576쪽. ISBN 978-1-4557-5980-4.
- ↑ 가 나 다 라 마 바 사 아 Powers AC (2005). Kasper DL, Braunwald E, Fauci AS, 외., 편집. 《Harrison's Principles of Internal Medicine》 16판. New York, NY: McGraw-Hill. 2152–2180쪽. ISBN 978-0-07-139140-5.
- ↑ Elzouki AY, Harfi HA, Nazer H, Oh W, Stapleton FB, Whitley RJ (2011). 《Textbook of Clinical Pediatrics》 (영어). Springer Science & Business Media. 2567쪽. ISBN 9783642022012.
- ↑ 가 나 다 라 Glaser N (June 2006). “New perspectives on the pathogenesis of cerebral edema complicating diabetic ketoacidosis in children”. 《Pediatric Endocrinology Reviews》 3 (4): 379–386. PMID 16816806.
- ↑ 가 나 다 라 마 Umpierrez GE, Smiley D, Kitabchi AE (March 2006). “Narrative review: ketosis-prone type 2 diabetes mellitus”. 《Annals of Internal Medicine》 144 (5): 350–357. doi:10.7326/0003-4819-144-5-200603070-00011. PMID 16520476. S2CID 33296818.
- ↑ 가 나 Goldenberg RM, Berard LD, Cheng AY, Gilbert JD, Verma S, Woo VC, Yale JF (December 2016). “SGLT2 Inhibitor-associated Diabetic Ketoacidosis: Clinical Review and Recommendations for Prevention and Diagnosis”. 《Clinical Therapeutics》 38 (12): 2654–2664.e1. doi:10.1016/j.clinthera.2016.11.002. PMID 28003053.
- ↑ Perry RJ, Rabin-Court A, Song JD, Cardone RL, Wang Y, Kibbey RG, Shulman GI (February 2019). “Dehydration and insulinopenia are necessary and sufficient for euglycemic ketoacidosis in SGLT2 inhibitor-treated rats”. 《Nature Communications》 10 (1): 548. doi:10.1038/s41467-019-08466-w. PMC 6358621. PMID 30710078.
- ↑ Milder DA, Milder TY, Kam PC (August 2018). “Sodium-glucose co-transporter type-2 inhibitors: pharmacology and peri-operative considerations”. 《Anaesthesia》 73 (8): 1008–1018. doi:10.1111/anae.14251. PMID 29529345.
- ↑ Danne T, Garg S, Peters AL, Buse JB, Mathieu C, Pettus JH, 외. (June 2019). “International Consensus on Risk Management of Diabetic Ketoacidosis in Patients With Type 1 Diabetes Treated With Sodium-Glucose Cotransporter (SGLT) Inhibitors”. 《Diabetes Care》 42 (6): 1147–1154. doi:10.2337/dc18-2316. PMC 6973545. PMID 30728224.
As a general guideline, SGLT-inhibitor therapy should not be used in patients using lowcarbohydrate or ketogenic diets as, anecdotally, they seem to be at increased risk of adverse ketosis effects
- ↑ 가 나 Kitabchi AE, Umpierrez GE, Murphy MB, Kreisberg RA (December 2006). “Hyperglycemic crises in adult patients with diabetes: a consensus statement from the American Diabetes Association”. 《Diabetes Care》 29 (12): 2739–2748. doi:10.2337/dc06-9916. PMID 17130218. 2010년 3월 27일에 원본 문서에서 보존된 문서.
- ↑ 가 나 다 라 마 바 Dunger DB, Sperling MA, Acerini CL, Bohn DJ, Daneman D, Danne TP, 외. (February 2004). “European Society for Paediatric Endocrinology/Lawson Wilkins Pediatric Endocrine Society consensus statement on diabetic ketoacidosis in children and adolescents”. 《Pediatrics》 113 (2): e133–e140. doi:10.1542/peds.113.2.e133. PMID 14754983. 2009년 9월 12일에 원본 문서에서 보존된 문서.
- ↑ 가 나 다 라 마 Brown TB (March 2004). “Cerebral oedema in childhood diabetic ketoacidosis: is treatment a factor?”. 《Emergency Medicine Journal》 21 (2): 141–144. doi:10.1136/emj.2002.001578. PMC 1726262. PMID 14988335.
- ↑ Klocker AA, Phelan H, Twigg SM, Craig ME (July 2013). “Blood β-hydroxybutyrate vs. urine acetoacetate testing for the prevention and management of ketoacidosis in Type 1 diabetes: a systematic review”. 《Diabetic Medicine》 30 (7): 818–824. doi:10.1111/dme.12136. PMID 23330615. S2CID 22070325.
- ↑ Misra S, Oliver NS (January 2015). “Utility of ketone measurement in the prevention, diagnosis and management of diabetic ketoacidosis”. 《Diabetic Medicine》 32 (1): 14–23. doi:10.1111/dme.12604. PMID 25307274. S2CID 11923923.
- ↑ 가 나 다 라 마 “Type 1 diabetes in adults: diagnosis and management”. National Institute for Health and Care Excellence. August 2015. 2016년 8월 9일에 원본 문서에서 보존된 문서. 2016년 2월 10일에 확인함.
- ↑ 가 나 다 라 마 바 사 Edge J (May 2009). “BSPED Recommended DKA Guidelines 2009” (PDF). British Society for Paediatric Endocrinology and Diabetes. 2011년 10월 27일에 원본 문서 (PDF)에서 보존된 문서. 2009년 7월 12일에 확인함.
- ↑ 가 나 Jayashree M, Williams V, Iyer R (2019). “Fluid Therapy For Pediatric Patients With Diabetic Ketoacidosis: Current Perspectives”. 《Diabetes, Metabolic Syndrome and Obesity: Targets and Therapy》 12: 2355–2361. doi:10.2147/DMSO.S194944. PMC 6858801. PMID 31814748.
- ↑ Andrade-Castellanos CA, Colunga-Lozano LE, Delgado-Figueroa N, Gonzalez-Padilla DA (January 2016). “Subcutaneous rapid-acting insulin analogues for diabetic ketoacidosis”. 《The Cochrane Database of Systematic Reviews》 1 (1): CD011281. doi:10.1002/14651858.CD011281.pub2. PMC 8829395. PMID 26798030.
- ↑ Silverstein J, Klingensmith G, Copeland K, Plotnick L, Kaufman F, Laffel L, 외. (January 2005). “Care of children and adolescents with type 1 diabetes: a statement of the American Diabetes Association”. 《Diabetes Care》 28 (1): 186–212. doi:10.2337/diacare.28.1.186. PMID 15616254. 2016년 4월 19일에 원본 문서에서 보존된 문서.
- ↑ Lindner LM, Rathmann W, Rosenbauer J (January 2018). “Inequalities in glycaemic control, hypoglycaemia and diabetic ketoacidosis according to socio-economic status and area-level deprivation in Type 1 diabetes mellitus: a systematic review”. 《Diabetic Medicine》 35 (1): 12–32. doi:10.1111/dme.13519. PMID 28945942. S2CID 24297858.
- ↑ Patel A, Singh D, Bhatt P, Thakkar B, Akingbola OA, Srivastav SK (September 2016). “Incidence, Trends, and Outcomes of Cerebral Edema Among Children With Diabetic Ketoacidosis in the United States”. 《Clinical Pediatrics》 55 (10): 943–951. doi:10.1177/0009922815617975. PMID 26603587. S2CID 25624176.
- ↑ Dreschfeld J (August 1886). “The Bradshawe Lecture on Diabetic Coma”. 《British Medical Journal》 2 (1338): 358–363. doi:10.1136/bmj.2.1338.358. PMC 2256374. PMID 20751675.
- ↑ 가 나 다 라 Kitabchi AE, Umpierrez GE, Fisher JN, Murphy MB, Stentz FB (May 2008). “Thirty years of personal experience in hyperglycemic crises: diabetic ketoacidosis and hyperglycemic hyperosmolar state”. 《The Journal of Clinical Endocrinology and Metabolism》 93 (5): 1541–1552. doi:10.1210/jc.2007-2577. PMC 2386681. PMID 18270259.
- ↑ Dillon ES, Riggs HE, Dyer WW (1936). “Cerebral lesions in uncomplicated fatal diabetic acidosis”. 《American Journal of the Medical Sciences》 192 (3): 360–365. doi:10.1097/00000441-193609000-00007. S2CID 72917358.
- ↑ Winter WE, Maclaren NK, Riley WJ, Clarke DW, Kappy MS, Spillar RP (February 1987). “Maturity-onset diabetes of youth in black Americans”. 《The New England Journal of Medicine》 316 (6): 285–291. doi:10.1056/NEJM198702053160601. PMID 3543673.