류코트리엔
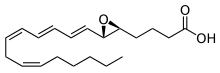
류코트리엔(leukotriene)은 아라키돈산 5-지질산소화효소에 의해 아라키돈산(AA)과 필수 지방산인 에이코사펜타엔산(EPA)이 산화되어 백혈구에서 생산하는 에이코사노이드 계열의 염증 매개 물질이다.[1][2][3] 류코트라이엔이라고도 한다.




류코트리엔은 면역 반응을 조절하기 위해 지질 신호 전달을 이용하여, 신호를 만든 세포 자기 자신(자가분비 신호)이나 이웃 세포(주변분비 신호)에 정보를 전달한다. 류코트리엔 생성은 일반적으로 염증 매개체로 같이 작용하는 히스타민이나 프로스타글란딘 생성을 동반한다.[4]
류코트리엔의 역할 중 하나(특히 LTD4)는 세기관지를 감싸고 있는 평활근의 수축을 유발하는 것이다. 류코트리엔의 과도한 생산은 천식과 알레르기성 비염에서 염증을 일으키는 주요 원인이다.[5] 항류코트리엔제는 류코트리엔의 생성이나 활성을 억제하여 이러한 호흡기 장애를 치료하는 데 사용된다.[6]
역사와 이름 편집
1979년 스웨덴 생화학자 벵트 잉에마르 사무엘손이 도입한 'leukotriene'이라는 이름은 백혈구(leukocyte)와 트리엔(화합물에 존재하는 3개의 공액 이중 결합을 뜻함)이라는 단어에서 유래했다. 나중에 류코트리엔 C로 명명된 '저속 평활근 자극 물질'(저속반응물질, SRS-A)은 원래 Feldberg와 Kellaway가 1938년에서 1940년 사이에 설명했다.[7][8][9] 연구자들은 뱀 독과 히스타민에 노출된 후 장기간이 지난 폐 조직에서 SRS를 분리해냈다.[10]
유형 편집
시스테이닐 류코트리엔 편집
LTC4, LTD4, LTE4, LTF4는 구조에 시스테인을 가지고 있기 때문에 종종 시스테이닐 류코트리엔(cisteinyl leukotriene)이라고 한다. 시스테이닐 류코트리엔은 SRS-A을 구성한다. LTD4와 마찬가지로 LTF4는 LTC4의 대사 산물이지만 글루타티온의 글루타민 잔기가 없는 LTD4와 달리 LTF4는 글루타티온의 글라이신 잔기가 없다.[11]
LTB4 편집
LTB4는 류코트리엔 A4 가수분해효소에 의해 LTA4로부터 생체내(in vivo)에서 합성된다. 주요 기능은 호중구를 조직 손상 부위로 동원하는 것이지만 다양한 면역 세포에 의한 염증성 사이토카인 생성을 촉진하는 데에도 도움이 된다. LTB4의 작용을 차단하는 약물은 호중구 매개 질환의 진행을 늦추는 데 약간의 효능을 보였다.[12]
LTG4 편집
시스테인 작용기가 알파케토산으로 산화된(즉 시스테인이 피루브산으로 대체된) LTE4의 대사산물인 LTG4의 존재도 가정되었다. 이 추정되는 류코트리엔에 대해 알려진 것은 거의 없다.
LTB5 편집
오메가-3 클래스 에이코사펜타엔산(EPA)에서 유래한 류코트리엔은 염증 효과를 감소시켰다. LTB5는 쥐 호중구의 응집, 인간 다형핵 호중구(PMN)의 화학운동성, 인간 PMN으로부터의 리소좀 효소 방출, 브라디키닌 유도 혈장 삼출을 강화시키지만, LTB4와 비교하여 적어도 30배 더 적은 효능을 가지고 있다.[13]
생화학 편집
합성 편집
류코트리엔은 아라키돈산 5-지질산소화효소에 의해 아라키돈산으로부터 세포에서 합성된다. 촉매 기전에는 아라키돈산 골격의 특정 위치에 산소 부분을 삽입하는 것이 있다.
지질산소화효소 경로는 백혈구와 비만 세포, 호산구, 호중구, 단핵구, 호염기구를 포함한 기타 면역 세포에서 활성화된다. 이러한 세포가 활성화되면 아라키돈산은 인지질분해효소 A2(PLA2)에 의해 세포막 인지질에서 유리되고 5-지질산소화효소 활성화 단백질(FLAP)에 의해 5-지질산소화효소로 주어진다.
5-지질산소화효소(5-LO)는 FLAP을 사용하여 아라키돈산을 아라키돈산 5-하이드로퍼옥사이드(5-HPETE)로 전환하고, 이는 자발적으로 5-하이드록시에이코사테트라엔산(5-HETE)으로 환원된다. 효소 5-LO는 5-HETE에 다시 작용하여 불안정한 에폭사이드인 류코트리엔 A4(LTA4)로 전환한다. 5-HETE는 추가로 5-oxo-ETE 및 5-oxo-15-hydroxy-ETE로 대사될 수 있으며, 이들 모두는 LTB4와 유사하지만 동일하지는 않은 전염증성 작용을 가진다. 또한 이 물질들은 LTB4 수용체에 의해 매개되지 않고 오히려 OXE 수용체에 의해 매개된다.[14][15]
호중구나 단핵구와 같은 류코트리엔 A4 가수분해효소가 있는 세포에서 LTA4는 다이하이드록시산 류코트리엔 LTB4로 전환되며, LTB4는 이들 세포의 원형질막에 있는 BLT1, BLT2 수용체에서 작용하는 호중구에 대한 강력한 화학주성 물질이다.
비만 세포나 호산구와 같은 류코트리엔 C4 합성효소를 발현하는 세포에서 LTA4는 트리펩타이드 글루타티온과 접합되어 첫 번째 시스테이닐-류코트리엔인 LTC4를 형성한다. 세포 외부에서 LTC4는 효소에 의해 전환되어 생물학적 활성을 유지하는 LTD4와 LTE4를 연속적으로 형성할 수 있다.
시스테이닐 류코트리엔은 표적 세포의 세포 표면 수용체 CysLT1과 CysLT2에 작용하여 기관지와 혈관 평활근을 수축시키고, 소혈관의 투과성을 증가시키며, 기도와 창자의 점액 분비를 증가시키고, 백혈구를 염증 부위로 동원한다.
LTB4와 시스테이닐 류코트리엔(LTC4, LTD4, LTE4)은 모두 국소 조직에서 부분적으로 분해되어 궁극적으로 간에서 비활성 대사 산물이 된다.
기능 편집
류코트리엔은 주로 G 단백질 연결 수용체(GPCR)의 서브패밀리에 작용한다. 또한 퍼옥시좀 증식자 활성화 수용체에도 작용할 수 있다. 류코트리엔은 천식과 알레르기 반응에 관여하고 염증 반응을 지속시키는 작용을 한다. 몬테루카스트나 자피르루카스트와 같은 여러 류코트리엔 수용체 길항제가 천식 치료에 사용된다. 최근 연구에서는 심혈관 질환과 신경 정신 질환에서 5-지질산소화효소의 역할을 주목하기도 했다.[16]
류코트리엔은 염증 반응에서 매우 중요한 약제이다. LTB4와 같은 일부 류코트리엔은 호중구 이동에 화학주성 효과가 있어 필요한 세포를 조직으로 가져오는 데 도움이 된다. 또한 류코트리엔은 기관지수축에 강력한 효과가 있으며 혈관 투과성을 증가시킨다.[17]
천식에서의 류코트리엔 편집
류코트리엔은 특히 아스피린 악화 호흡기 질환(AERD) 환자에서 천식의 발병기전에 관여하고 다음의 증상을 유발하거나 강하게 한다.[18]
- 기류 폐쇄
- 점액 분비 증가
- 점막 축적
- 기관지 수축
- 기도벽의 염증 세포 침윤
시스테이닐 류코트리엔의 역할 편집
시스테이닐 류코트리엔 수용체 CysLTR1과 CysLTR2는 비만 세포, 호산구, 내피세포에 존재한다. 시스테이닐 류코트리엔의 상호작용 동안 이들은 비만 세포에 의한 내피 세포 부착과 케모카인 생성 등 염증 유발 활성을 일으킬 수 있다. 또한 염증을 매개할 뿐만 아니라 천식이나 기타 염증성 장애를 유발하여 폐포로의 기류를 감소시킨다. 8-아이소프로스탄과 함께 시스테이닐 류코트리엔 수치가 천식 환자의 호기 응축물(EBC)에서 증가하는 것으로 보고되었으며 이는 질병의 중증도와 관련이 있다.[19] 또한 시스테이닐 류코트리엔은 일반적으로 약물 부작용, 특히 조영제 유발 부작용에서 역할을 할 수 있다.[20]
치매에서의 류코트리엔 편집
류코트리엔은 동물 연구에서 알츠하이머병과 관련된 치매의 후기 단계에서 중요한 역할을 하는 것으로 밝혀졌다. 타우 병리를 일으키는 타우 전이유전자를 가진 마우스에서 5-지질산소화효소를 차단하여 류코트리엔 형성을 억제하는 약물인 질루톤이 기억상실을 역전시키는 것으로 밝혀졌다.[22]
참고 문헌 편집
- ↑ Loick, H.; Theissen, J. (1994). “Die Eicosanoide als Mediatoren beim ARDS” [Eicosanoids as mediators in ARDS]. 《Anästhesiologie, Intensivmedizin, Notfallmedizin, Schmerztherapie》 (독일어) 29 (1): 3–9. doi:10.1055/s-2007-996677. PMID 8142566.
- ↑ Salmon, John A; Higgs, Gerald A (1987). “Prostaglandins and leukotrienes as inflammatory mediators”. 《British Medical Bulletin》 43 (2): 285–96. doi:10.1093/oxfordjournals.bmb.a072183. PMID 2825898.
- ↑ O'Byrne, Paul M.; Israel, Elliot; Drazen, Jeffrey M. (1997). “Antileukotrienes in the treatment of asthma”. 《Annals of Internal Medicine》 127 (6): 472–80. doi:10.7326/0003-4819-127-6-199709150-00009. PMID 9313005.
- ↑ White, Martha (1999). “Mediators of inflammation and the inflammatory process”. 《The Journal of Allergy and Clinical Immunology》 103 (3 Pt 2): S378-81. doi:10.1016/S0091-6749(99)70215-0. PMID 10069896. 2019년 6월 8일에 확인함.
- ↑ Nelson, David L.; Cox, Michael M. (2008). 〈Leukotrienes〉. 《Lehninger Principles of Biochemistry》 5판. Macmillan. 359쪽. ISBN 978-0-7167-7108-1.
- ↑ “Antileukotriene agents for the treatment of lung disease”. 《Am. J. Respir. Crit. Care Med.》 188 (5): 538–544. September 2018. doi:10.1164/rccm.201301-0023PP. PMID 23822826.
- ↑ Feldberg, W.; Kellaway, C. H. (1938). “Liberation of histamine and formation of lysocithin-like substances by cobra venom”. 《The Journal of Physiology》 94 (2): 187–226. doi:10.1113/jphysiol.1938.sp003674. PMC 1393616. PMID 16995038.
- ↑ Feldberg, W.; Holden, H. F.; Kellaway, C. H. (1938). “The formation of lysocithin and of a muscle-stimulating substance by snake venoms”. 《The Journal of Physiology》 94 (2): 232–48. doi:10.1113/jphysiol.1938.sp003676. PMC 1393612. PMID 16995040.
- ↑ Kellaway, C. H.; Trethewie, E. R. (1940). “The Liberation of a Slow‐Reacting Smooth Muscle‐Stimulating Substance in Anaphylaxis”. 《Quarterly Journal of Experimental Physiology and Cognate Medical Sciences》 30 (2): 121–45. doi:10.1113/expphysiol.1940.sp000825.
- ↑ Kellaway, C. H.; Trethewie, E. R. (1940). “The Liberation of a Slow-Reacting Smooth Muscle-Stimulating Substance in Anaphylaxis”. 《Quarterly Journal of Experimental Physiology and Cognate Medical Sciences》 (영어) 30 (2): 121–145. doi:10.1113/expphysiol.1940.sp000825. ISSN 1469-445X.
- ↑ internet checked April 24, 2012
- ↑ Crooks, S.W; Stockley, R.A (1998). “Leukotriene B4”. 《The International Journal of Biochemistry & Cell Biology》 30 (2): 173–8. doi:10.1016/S1357-2725(97)00123-4. PMID 9608670.
- ↑ Terano, Takashi; Salmon, John A.; Moncada, Salvador (1984). “Biosynthesis and biological activity of leukotriene B5”. 《Prostaglandins》 27 (2): 217–32. doi:10.1016/0090-6980(84)90075-3. PMID 6326200.
- ↑ O'Flaherty, Joseph T.; Taylor, Jennifer S.; Thomas, Michael J. (1998). “Receptors for the 5-oxo class of eicosanoids in neutrophils”. 《The Journal of Biological Chemistry》 273 (49): 32535–41. doi:10.1074/jbc.273.49.32535. PMID 9829988.
- ↑ Powell, William S.; Rokach, Joshua (2013). “The eosinophil chemoattractant 5-oxo-ETE and the OXE receptor”. 《Progress in Lipid Research》 52 (4): 651–65. doi:10.1016/j.plipres.2013.09.001. PMC 5710732. PMID 24056189.
- ↑ Manev, Radmila; Manev, Hari (2004). “5-Lipoxygenase as a Putative Link Between Cardiovascular and Psychiatric Disorders”. 《Critical Reviews in Neurobiology》 16 (1–2): 181–6. doi:10.1615/CritRevNeurobiol.v16.i12.190. PMID 15581413.
- ↑ Dahlén, Sven-Erik; Björk, Jakob; Hedqvist, Per; Arfors, Karl-E.; Hammarström, Sven; Lindgren, Jan-Åke; Samuelsson, Bengt (1981). “Leukotrienes promote plasma leakage and leukocyte adhesion in postcapillary venules: in vivo effects with relevance to the acute inflammatory response”. 《Proceedings of the National Academy of Sciences》 78 (6): 3887–91. Bibcode:1981PNAS...78.3887D. doi:10.1073/pnas.78.6.3887. JSTOR 10943. PMC 319678. PMID 6267608.
- ↑ Berger, A. (1999). “Science commentary: What are leukotrienes and how do they work in asthma?”. 《BMJ》 319 (7202): 90. doi:10.1136/bmj.319.7202.90. PMC 1116241. PMID 10398630.
- ↑ Samitas, Konstantinos; Chorianopoulos, Dimitrios; Vittorakis, Stelios; Zervas, Eleftherios; Economidou, Erasmia; Papatheodorou, George; Loukides, Stelios; Gaga, Mina (2009). “Exhaled cysteinyl-leukotrienes and 8-isoprostane in patients with asthma and their relation to clinical severity”. 《Respiratory Medicine》 103 (5): 750–6. doi:10.1016/j.rmed.2008.11.009. PMID 19110408.
- ↑ Böhm, Ingrid; Speck, Ulrich; Schild, Hans (2005). “A possible role for cysteinyl-leukotrienes in non-ionic contrast media induced adverse reactions”. 《European Journal of Radiology》 55 (3): 431–6. doi:10.1016/j.ejrad.2005.01.007. PMID 16129253.
- ↑ Brocklehurst, W. E. (1960). “The release of histamine and formation of a slow-reacting substance (SRS-A) during anaphylactic shock”. 《The Journal of Physiology》 151 (3): 416–35. doi:10.1113/jphysiol.1960.sp006449. PMC 1363273. PMID 13804592.
- ↑ “Temple researchers reverse cognitive impairments in mice with dementia”. 《Eurekalart!》. 2018년 6월 8일.
추가 자료 편집
- Bailey, J. Martyn (1985) Prostaglandins, leukotrienes, and lipoxins: biochemistry, mechanism of action, and clinical applications Plenum Press, New York, ISBN 0-306-41980-7
- Lipkowitz, Myron A. and Navarra, Tova (2001) The Encyclopedia of Allergies (2nd ed.) Facts on File, New York, p. 167, ISBN 0-8160-4404-X
- Samuelsson, Bengt (ed.) (2001) Advances in prostaglandin and leukotriene research: basic science and new clinical applications: 11th International Conference on Advances in Prostaglandin and Leukotriene Research: Basic Science and New Clinical Applications, Florence, Italy, June 4–8, 2000 Kluwer Academic Publishers, Dordrecht, ISBN 1-4020-0146-0
외부 링크 편집
- 위키미디어 공용에 류코트리엔 관련 미디어 분류가 있습니다.
- 의학주제표목 (MeSH)의 Leukotrienes