아밀로이드 베타
알츠하이머 병에 관여하는 아미노산 펩타이드
(베타 아밀로이드에서 넘어옴)
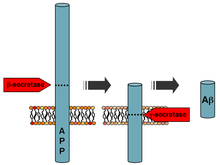
아밀로이드 베타 (Aβ 또는 A베타)는 알츠하이머 환자의 뇌에서 발견되는 아밀로이드 플라크의 주성분으로서 알츠하이머 병에 결정적으로 관여하는 36-43개의 아미노산 펩타이드를 의미한다.[2] 이 펩타이드는 베타 세크리타제와 감마 세크레타제에 의해 분해되어 Aβ를 생성하는, 아밀로이드 전구체 단백질 (APP)에서 유도된다. Aβ 분자는 응집되어 여러 형태로 존재할 수 있는 가용성 올리고머를 형성할 수 있다. ("씨앗"이라 알려진) 특정 잘못 접힌 올리고머가, 다른 Aβ 분자가 잘못 접힌 올리고머 형태를 유도하여 프리온 감염과 유사한 연쇄 반응을 유도할 수 있다고 오늘날 믿어진다. 씨앗 또는 그 결과 아밀로이드 플라크는 신경 세포에 독성이 있다. 알츠하이머 병에 관여하는 다른 단백질인 타우 단백질도 프리온처럼 잘못 접힌 올리고머를 형성하며 잘못 접힌 Aβ가 타우를 잘못 변형시킬 수 있다는 증거가 있다.[3][4]
| 아밀로이드 베타 펩타이드 (베타-APP) | |||||||||
|---|---|---|---|---|---|---|---|---|---|
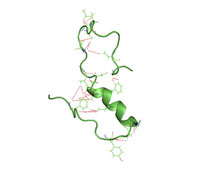 수성 환경에서 아밀로이드 베타(1 40)의 부분적으로 접힌 구조 (pdb 2lfm)[1] | |||||||||
| 식별자 | |||||||||
| 상징 | APP | ||||||||
| Pfam | PF03494 | ||||||||
| InterPro | IPR013803 | ||||||||
| SCOP | 2lfm | ||||||||
| SUPERFAMILY | 2lfm | ||||||||
| TCDB | 1.C.50 | ||||||||
| OPM superfamily | 369 | ||||||||
| OPM protein | 2y3k | ||||||||
| |||||||||
| 아밀로이드 베타 (A4) 전구 단백질 (펩티다제 넥신-II, 알츠하이머 병) | |||||||
|---|---|---|---|---|---|---|---|
 | |||||||
| 식별자 | |||||||
| 상징 | APP | ||||||
| NCBI 유전자 | 351 | ||||||
| HGNC | 620 | ||||||
| OMIM | 104760 | ||||||
| RefSeq | NM_000484 | ||||||
| UniProt | P05067 | ||||||
| 다른 정보 | |||||||
| 유전자 자리 | Chr. 21 q21.2 | ||||||
| |||||||
최근 연구에 따르면 APP와 그 아밀로이드 잠재력은 고대 기원의 것으로, 초기 후구동물 시대까지 거슬러 올라간다.[5]
최근, 베타 아밀로이드 가설 수립에 있어 또 다른 전기를 마련한 비임상 연구 논문에 이미지 데이터 일부가 조작됐다는 의혹이 제기되었다.[6]
출처 편집
- ↑ Vivekanandan S, Brender JR, Lee SY, Ramamoorthy A (Jul 2011). “A partially folded structure of amyloid-beta(1-40) in an aqueous environment”. 《Biochemical and Biophysical Research Communications》 411 (2): 312–6. doi:10.1016/j.bbrc.2011.06.133. PMC 3148408. PMID 21726530.
- ↑ Hamley IW (2012). “The Amyloid Beta Peptide: A Chemist’s Perspective. Role in Alzheimer’s and Fibrillization”. 《Chemical Reviews》 112: 5147–5192. doi:10.1021/cr3000994. PMID 22813427.
- ↑ Nussbaum JM, Seward ME, Bloom GS (Jan–Feb 2013). “Alzheimer disease: a tale of two prions”. 《Prion》 7 (1): 14–9. doi:10.4161/pri.22118. PMC 3609044. PMID 22965142.
- ↑ Pulawski W, Ghoshdastider U, Andrisano V, Filipek S (Apr 2012). “Ubiquitous amyloids”. 《Applied Biochemistry and Biotechnology》 166 (7): 1626–43. doi:10.1007/s12010-012-9549-3. PMC 3324686. PMID 22350870.
- ↑ Tharp WG, Sarkar IN (April 2013). “Origins of amyloid-β”. 《BMC Genomics》 14 (1): 290. doi:10.1186/1471-2164-14-290. PMC 3660159. PMID 23627794.
- ↑ “|포커스| 흔들리는 '베타 아밀로이드 가설'…찻잔속 태풍일까”. 2022년 7월 25일. 2022년 8월 22일에 확인함.
참고 도서 편집
- Martins IC, Kuperstein I, Wilkinson H, Maes E, Vanbrabant M, Jonckheere W, Van Gelder P, Hartmann D, D'Hooge R, De Strooper B, Schymkowitz J, Rousseau F (Jan 2008). “Lipids revert inert Aβ amyloid fibrils to neurotoxic protofibrils that affect learning in mice”. 《The EMBO Journal》 27 (1): 224–33. doi:10.1038/sj.emboj.7601953. PMC 2206134. PMID 18059472.
- Istrate AN, Tsvetkov PO, Mantsyzov AB, Kulikova AA, Kozin SA, Makarov AA, Polshakov VI (Jan 2012). “NMR solution structure of rat aβ(1-16): toward understanding the mechanism of rats' resistance to Alzheimer's disease”. 《Biophysical Journal》 102 (1): 136–43. Bibcode:2012BpJ...102..136I. doi:10.1016/j.bpj.2011.11.4006. PMC 3250693. PMID 22225807.
- Istrate AN, Kozin SA, Zhokhov SS, Mantsyzov AB, Kechko OI, Pastore A, Makarov AA, Polshakov VI (Feb 2016). “Interplay of histidine residues of the Alzheimer's disease Aβ peptide governs its Zn-induced oligomerization”. 《Scientific Reports》 6: 21734. doi:10.1038/srep21734. PMC 4761979. PMID 26898943.