산화 철(III)
화합물
(산화제이철에서 넘어옴)
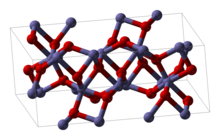
산화 철(III)(Iron(III) oxide, ferric oxide)은 산화 철의 일종으로, 화학식은 Fe2O3이다.
| |

| |

| |
| 이름 | |
|---|---|
| IUPAC 이름
Iron(III) oxide
| |
| 별칭 | |
| 식별자 | |
3D 모델 (JSmol)
|
|
| ChEBI | |
| ChemSpider | |
| ECHA InfoCard | 100.013.790 |
| EC 번호 |
|
| E 번호 | E172(ii) (착색제) |
| 11092 | |
| KEGG | |
PubChem CID
|
|
| RTECS 번호 |
|
| UNII | |
CompTox Dashboard (EPA)
|
|
| |
| 성질 | |
| Fe2O3 | |
| 몰 질량 | 159.687 g·mol−1 |
| 겉보기 | Red-brown solid |
| 냄새 | Odorless |
| 밀도 | 5.25 g/cm3[1] |
| 녹는점 | 1,539 °C (2,802 °F; 1,812 K)[1] decomposes 105 °C (221 °F; 378 K) β-dihydrate, decomposes 150 °C (302 °F; 423 K) β-monohydrate, decomposes 50 °C (122 °F; 323 K) α-dihydrate, decomposes 92 °C (198 °F; 365 K) α-monohydrate, decomposes[2] |
| Insoluble | |
| 용해도 | Soluble in diluted acids,[1] sugar solution Trihydrate slightly soluble in aq. tartaric acid, citric acid, CH3COOH[2] |
자화율 (χ)
|
+3586.0·10−6 cm3/mol |
굴절률 (nD)
|
n1=2.91, n2=3.19 (α, hematite)[3] |
| 구조 | |
| Rhombohedral, hR30 (α-form)[4] Cubic bixbyite, cI80 (β-form) Cubic spinel (γ-form) Orthorhombic (ε-form)[5] | |
| R3c, No. 161 (α-form)[4] Ia3, No. 206 (β-form) Pna21, No. 33 (ε-form)[5] | |
| 3m (α-form)[4] 2/m 3 (β-form) mm2 (ε-form)[5] | |
| Octahedral (Fe3+, α-form, β-form)[4] | |
| 열화학[6] | |
열용량 (C)
|
103.9 J/mol·K[6] |
표준 몰 엔트로피 (S
|
87.4 J/mol·K[6] |
표준 생성 엔탈피 (ΔfH⦵298)
|
−824.2 kJ/mol[6] |
기브스 자유 에너지 (ΔfG˚)
|
−742.2 kJ/mol[6] |
| 위험 | |
| GHS 그림문자 |  [7] [7]
|
| 신호어 | 경고 |
| H315, H319, H335[7] | |
| P261, P305+351+338[7] | |
| NFPA 704 (파이어 다이아몬드) | |
유해화학물질 허용농도 (TLV)
|
5 mg/m3[1] (TWA) |
| 반수 치사량 또는 반수 치사농도 (LD, LC): | |
LD50 (median dose)
|
10 g/kg (rats, oral)[9] |
| NIOSH (미국 건강 노출 한계): | |
PEL (허용)
|
TWA 10 mg/m3[8] |
REL (권장)
|
TWA 5 mg/m3[8] |
IDLH (직접적 위험)
|
2500 mg/m3[8] |
| 관련 화합물 | |
다른 음이온
|
Iron(III) fluoride |
다른 양이온
|
Manganese(III) oxide Cobalt(III) oxide |
관련 iron oxides
|
Iron(II) oxide Iron(II,III) oxide |
달리 명시된 경우를 제외하면, 표준상태(25 °C [77 °F], 100 kPa)에서 물질의 정보가 제공됨.
| |
적철석 편집
천연으로는 적철석(赤鐵石)으로서 널리 산출되며, 적색토양의 빛깔의 요인이다. 적갈색 분말로, 비중 4.5∼5.2, 녹는점 1,550℃, 흡유량(吸油量) 22∼75 %이다. 햇빛 ·공기 ·수분 ·열 등에 대하여 상당히 안정하며, 한번 가열한 것은 잘 녹지 않는다. 자성을 보인다. 철을 공기 속에서 가열하면 생긴다.
제조 편집
예전에는 황산철[綠礬]을 구워서 만들었으나, 최근에는 철강공업이나 도금공업의 폐액(廢液)에서 생긴 황산철을 원료로 하여 만든다. 제조법에 따라 적색인 것에서 황색 ·갈색 ·자색 ·흑색 등을 띠는데, 빛깔이 다른 원인으로서는 입자의 크기, 혼입물의 종류, 결정격자(結晶格子)의 완전성 등을 들 수 있다.
용도 편집
공업적으로는 벵갈라라는 적색 안료(顔料)로서, 또 유리 ·귀금속 ·다이아몬드의 연마재(硏磨材)로서 사용된다. 순도가 높은 것은 반도체로 사용되고, 또 마그넷 ·자기(磁氣)테이프의 원료로도 쓰인다.[10]
같이 보기 편집
각주 편집
- ↑ 가 나 다 라 Haynes, p. 4.69
- ↑ 가 나 Comey, Arthur Messinger; Hahn, Dorothy A. (February 1921). 《A Dictionary of Chemical Solubilities: Inorganic》 2판. New York: The MacMillan Company. 433쪽.
- ↑ Haynes, p. 4.141
- ↑ 가 나 다 라 Ling, Yichuan; Wheeler, Damon A.; Zhang, Jin Zhong; Li, Yat (2013). Zhai, Tianyou; Yao, Jiannian, 편집. 《One-Dimensional Nanostructures: Principles and Applications》. 《John Wiley & Sons, Inc.》 (Hoboken, New Jersey: John Wiley & Sons, Inc.). 167쪽. ISBN 978-1-118-07191-5.
- ↑ 가 나 다 Vujtek, Milan; Zboril, Radek; Kubinek, Roman; Mashlan, Miroslav. “Ultrafine Particles of Iron(III) Oxides by View of AFM – Novel Route for Study of Polymorphism in Nano-world” (PDF). 《Univerzity Palackého》. Czech. 2014년 7월 12일에 확인함.
- ↑ 가 나 다 라 마 Haynes, p. 5.12
- ↑ 가 나 다 Sigma-Aldrich Co. Retrieved on 2014-07-12.
- ↑ 가 나 다 NIOSH Pocket Guide to Chemical Hazards. “#0344”. 미국 국립 직업안전위생연구소 (NIOSH).
- ↑ 가 나 “SDS of Iron(III) oxide” (PDF). 《KJLC》. England: Kurt J Lesker Company Ltd. 2012년 1월 5일. 2014년 7월 12일에 확인함.
- ↑ “[네이버 지식백과] 산화철 [iron oxide, 酸化鐵] (두산백과)”.
| 이 글은 화학에 관한 토막글입니다. 여러분의 지식으로 알차게 문서를 완성해 갑시다. |
