위키백과:과학의 달 에디터톤/2022년/심사표/인산염
여기에 위키 문법을 사용하지 않을 글을 적어 주세요
| |||
| |||
| 이름 | |||
|---|---|---|---|
| 체계명
Phosphate[1] | |||
| 식별자 | |||
3D 모델 (JSmol)
|
|||
| 3903772 | |||
| ChEBI | |||
| ChemSpider | |||
| 1997 | |||
| MeSH | Phosphates | ||
PubChem CID
|
|||
| UNII | |||
| |||
| |||
| 성질 | |||
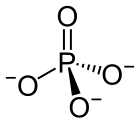
| PO3− 4 | |||
| 몰 질량 | 94.9714 g mol−1 | ||
| 짝산 | Monohydrogen phosphate | ||
달리 명시된 경우를 제외하면, 표준상태(25 °C [77 °F], 100 kPa)에서 물질의 정보가 제공됨.
| |||
Tracking categories (test):
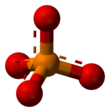
인산염(燐酸鹽, 영어: phosphate)은 인산의 염을 가리키는 무기 화합물이다. 하나의 인과 4개의 산소로 구성된 다원자 이온 또는 근본 물질에서 형성된 물질이다. 인산 이온(phosphate ion)은 −3 값의 전하를 가지고 PO43-로 써서 나타낸다. 다시 말해 인산에 있는 수소 이온을 금속 이온 따위의 양이온으로 치환한 염을 가리킨다. 인산염을 이용하면 농업과 공업에 쓰이는 인을 얻을 수 있고, 식품 첨가물로도 사용된다.
특성 편집
-
H
3PO
4 -
H
2PO−
4 -
HPO2−
4 -
PO3−
4
- 세 가지 반응
- 25 °C 환경 (mol/L)
- (pKa1 2.12)
- (pKa2 7.21)
- (pKa3 12.67)
용해 편집
- 1산성염인 이차염과 정염인 삼차염은 알칼리염만 물에 녹는다.
- 2산성염인 일차염은 모두 물에 녹는다.
같이 보기 편집
각주 편집
- ↑ “Phosphates – PubChem Public Chemical Database”. 《The PubChem Project》. USA: National Center of Biotechnology Information.
외부 링크 편집
- 위키미디어 공용에 과학의 달 에디터톤/2022년/심사표/인산염 관련 미디어 분류가 있습니다.
- (영어) 과학의 달 에디터톤/2022년/심사표/인산염 - PubChem
- (영어) US Minerals Databrowser provides data graphics covering consumption, production, imports, exports and price for phosphate and 86 other minerals