바이러스 잠복
바이러스 잠복(Virus latency)은 병리적 바이러스가 세포 내에서 휴면상태로 잠복해있는 용원성 생활사의 한 단계를 말한다.[1] 잠복 감염은 만성 감염과 달리 바이러스가 검출되지 않으며, 바이러스 입자의 증식은 중단되었으나 유전체는 체내에 남아있는 상태이다.[2][3] 따라서 면역 약화 등 환경이 갖춰지면 언제든지 재활성화되어 세포가 바이러스에 따로 감염되지 않아도 용균성 생활사를 가지는 바이러스를 생성할 수 있게 된다.[4]
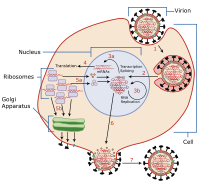 |
의료적인 용어로써 잠복기는 바이러스가 휴면상태에 있음을 의미하지 않는다는 점에서 바이러스 잠복과 다르다.
기작
에피좀 잠복
에피좀 잠복은 에피좀의 형태로 이루어지는 바이러스 잠복의 한 형태를 말한다. 이 경우 바이러스 유전자는 세포질이나 세포핵에서 숙주세포의 유전체와 별개의 안정된 유전체나 인트론으로 존재한다. 에피좀 잠복은 프로바이러스성 잠복보다 숙주세포의 리보자임이나 외래 유전자 파괴 기작에 더욱 취약하다.
단순포진바이러스과에 속한 모든 바이러스들은 잠복 감염을 한다. 특히 수두대상포진바이러스와 단순포진바이러스(HSV-1, HSV-2)는 신경 세포에 잠복하여 세포질에 선형 유전체를 남긴다.[5] 감마헤르페스아과는 면역계 세포에서 잠복하며 그중 하나인 엡스타인-바 바이러스는 B세포에서 잠복하는데,[5][6] 이 바이러스는 화학요법이나 방사선치료 등의 이유로 인해 용균성 생활사를 따르게 되면 유전체 불안정과 암을 야기할 수 있다.[7] 단순포진바이러스(HSV)의 유전체는 신경 아교 세포나[8] 뇌세포 등의 신경세포의 DNA에 섞여들어가며, 염색질이 산소나 영양소 부족으로 인해[9] 조금이라도 풀어지면 재활성화된다.[10]
거대세포바이러스(CMV)는 골수성 전구세포에 잠복하며 염증으로 재활성화된다.[11] 면역억제나 패혈증 등의 심각한 질병 역시 CMV의 재활성화를 야기한다.[12] 대장암 환자에게서도 CMV 재활성화가 흔하게 이루어진다.[13]
유전체가 꼭 핵에 들어갈 필요가 없으므로 핵체가 인터페론을 활성화하는것을 방지할 수 있다는 장점이 있으나, 다른 세포 방어기작에 더 많이 노출되어 효소에 의해 파괴될 수 있다는 점이 있다.[14] 자외선 등 외부 스트레스 요인으로 인해 재활성화될 수 있다.[15]
프로바이러스성 장복
프로바이러스는 숙주세포의 DNA와 합쳐진 상태의 바이러스 유전체를 부르는 말이다. 숙주세포가 분열할 때 자동으로 복제되며, 세포를 죽이지 않는 이상 감염된 프로바이러스를 제거할 방법이 마땅치 않다는 장점이 있다.[16] 그러나 핵 내부로 들어가야하며 이를 위해 별도의 단백질들이 필요하다는 단점이 있다. 그러나 일단 한번 프로바이러스의 형태로 전환되고나서는 세포가 살아있는 동안 영속할 수 있다.
인간면역결핍 바이러스가 가장 대표적이다. 이 바이러스는 역전사하여 RNA 유전체로부터 DNA를 만들고, 프로바이러스의 형태로 잠복하여 면역계로부터 거의 완벽하게 숨는다. 또한 다른 잠복 바이러스들과 동일하게 잠복중에는 증상을 나타내지 않는다. 불행하게도 프로바이러스 상태의 항역전사 약물로 프로바이러스 형태의 인간면역결핍 바이러스를 표적하기란 불가능에 가깝다.
유지 잠복
프로바이러스성 잠복과 에피좀 잠복은 모두 감염상태를 유지하며 바이러스 유전자를 보존해야한다는 공통점이 있다. 따라서 잠복중인 바이러스 유전자는 자기 자신을 유지하기 위해 발현된다. 이런 잠복연관(latency-associated) 유전자의 발현은 유전체가 리보자임이나 면역계에 의해 발견되어 소화되는 것을 방지한다. 특히 어떤 비암호화 RNA들이나 단백질들은 아폽토시스를 억제하거나 유사 분열을 촉진하여 감염된 세포가 더 많이 존재하게한다.[17] 단순포진바이러스의 경우 잠복연관전사체(- transcripts, LAT)가 주조직 적합성 복합체 등의 아폽토시스 유발인자들을 억제함으로써 아폽토시스가 이루어지지 못하게한다.[18]
내재성 레트로바이러스는 과거에 이런 잠복능력을 갖췄을 것으로 여겨진다. 이 바이러스들은 먼 과거에 인간 유전체에 통합되어, 현재는 인간의 생식과 함께 번식한다. 이런 유전자는 대부분 매우 많은 진화단계 거쳐 발현능력을 상실하였다.[19] 일부 유전자의 경우 현재에도 발현되는데, 이들은 숙주세포와 같이 진화하여 숙주세포의 정상적 기능에 편입되어 중요한 기능을 수행한다.[20]
영향
바이러스 잠복중에는 바이러스 배출이나 병리학적 증상을 나타내지 않지만, 외부 스트레스가 주어진다면 재활성되어 급성 감염을 일으킬 수 있다. 대부분의 사람이 감염되어있는 단순포진바이러스의 한 혈청형은 재활성화되면 구순포진을 일으킨다. 수두대상포진바이러스의 경우 초기 급성 감염 이후 계속 잠복해있다가 재활성화되어 대상포진을 일으킨다.
잠복감염이 세포를 변형시켜 통제되지않는 세포분열을 야기하는 경우도 있다. 이는 특히 숙주 유전체내의 무작위적인 삽입이 숙주세포의 성장인자 등을 오염시킴으로써 발생한다. 파리의 네커 병원(Necker Hospital)에서 유전병으로 유전자 치료를 받던 20세 남성이 백혈병을 가지게 된 사례가 대표적이다.[21]
인간 유두종바이러스의 지속감염이 악성변환의 결과로 자궁경부암을 야기한 경우도 보고되었다.[22][23][24]
인간면역결핍 바이러스의 경우 긴 수명을 가진 세포 내에서 프로바이러스성 잠복을 하는데, 아무리 길게 항레트로바이러스성 약물을 투여한다고 해도 멀쩡히 남아있다.[25] 잠복장소의 긴 수명이 항바이러스제 치료의 어려움을 설명해준다.[25][26][27][28]
같이 보기
각주
- ↑ Villarreal, Luis P. (2005). Viruses and the Evolution of Life. Washington, ASM Press.
- ↑ “시간에 의한 분류”. 2020년 4월 18일에 확인함.
- ↑ “잠복감염”. 2020년 4월 18일에 확인함.
- ↑ N.J. Dimmock et al. "Introduction to Modern Virology, 6th edition." Blackwell Publishing, 2007.
- ↑ 가 나 Minarovits J (2006). 〈Epigenotypes of Latent Herpesvirus Genomes〉. 《DNA Methylation: Development, Genetic Disease and Cancer》. Current Topics in Microbiology and Immunology 310. 61–80쪽. doi:10.1007/3-540-31181-5_5. ISBN 978-3-540-31180-5. PMID 16909907.
- ↑ Souza TA, Stollar BD, Sullivan JL, Luzuriaga K, Thorley-Lawson DA (2007년 9월 1일). “Influence of EBV on the peripheral blood memory B cell compartment”. 《Journal of Immunology》 179 (5): 3153–60. doi:10.4049/jimmunol.179.5.3153. PMID 17709530.
- ↑ Li H, Liu S, Hu J, Luo X, Li N, M Bode A, Cao Y (2016). “Epstein-Barr virus lytic reactivation regulation and its pathogenic role in carcinogenesis”. 《International Journal of Biological Sciences》 12 (11): 1309–1318. doi:10.7150/ijbs.16564. PMC 5118777. PMID 27877083.
- ↑ Thellman NM, Triezenberg SJ (2017). “Herpes Simplex Virus Establishment, Maintenance, and Reactivation: In Vitro Modeling of Latency”. 《Pathogens》 6 (3): E28. doi:10.3390/pathogens6030028. PMC 5617985. PMID 28644417.
- ↑ “Starve a Cell, Compact Its DNA - GEN”. 《GEN》. 2015년 11월 10일.
- ↑ “Discovery shows how herpes simplex virus reactivates in neurons to trigger disease”. 2015년 12월 21일.
- ↑ Dupont L, Reeves MB (2016). “Cytomegalovirus latency and reactivation: recent insights into an age old problem”. 《Reviews in Medical Virology》 26 (2): 75–89. doi:10.1002/rmv.1862. PMC 5458136. PMID 26572645.
- ↑ Cook CH (2007). “Cytomegalovirus reactivation in "immunocompetent" patients: a call for scientific prophylaxis”. 《The Journal of Infectious Diseases》 196 (9): 1273–1275. doi:10.1086/522433. PMID 17922387.
- ↑ Sager K, Alam S, Bond A, Chinnappan L, Probert CS (2015). “Review article: cytomegalovirus and inflammatory bowel disease”. 《Alimentary Pharmacology & Therapeutics》 41 (8): 725–733. doi:10.1111/apt.13124. PMID 25684400.
- ↑ Burton EA, Fink DJ, Glorioso JC (Dec 2002). “Gene delivery using herpes simplex virus vectors”. 《DNA Cell Biol》 21 (12): 915–36. doi:10.1089/104454902762053864. PMID 12573050.
- ↑ Preston, Chris M.; Efstathiou, Stacey (2018년 9월 21일). 〈Molecular basis of HSV latency and reactivation〉. Arvin, Ann; Campadelli-Fiume, Gabriella; Mocarski, Edward; Moore, Patrick S.; Roizman, Bernard; Whitley, Richard; Yamanishi, Koichi. 《Human Herpesviruses: Biology, Therapy, and Immunoprophylaxis》. Cambridge University Press. ISBN 9780521827140. PMID 21348106 – PubMed 경유.
- ↑ Marcello A. "Latency: the hidden HIV-1 challenge." Retrovirology. 2006 Jan 16;3(1):7
- ↑ Divito S, Cherpes TL, Hendricks RL (2006). “A triple entente: virus, neurons, and CD8+ T cells maintain HSV-1 latency”. 《Immunol. Res.》 36 (1–3): 119–26. doi:10.1385/ir:36:1:119. PMID 17337772.
- ↑ Carpenter D, Hsiang C, Brown DJ, Jin L, Osorio N, Benmohamed L, Jones C, Wechsler SL (Dec 2007). “Stable cell lines expressing high levels of the herpes simplex virus type 1 LAT are refractory to caspase 3 activation and DNA laddering following cold shock induced apoptosis”. 《Virology》 369 (1): 12–8. doi:10.1016/j.virol.2007.07.023. PMC 2276668. PMID 17727910.
- ↑ Buzdin A (Nov 2007). “Human-specific endogenous retroviruses”. 《ScientificWorldJournal》 7: 1848–68. doi:10.1100/tsw.2007.270. PMC 5901341. PMID 18060323.
- ↑ Hayashida K, Omagari K, Masuda JI, Kohno S (2007). “An integrase of endogenous retrovirus is involved in maternal mitochondrial DNA inheritance of the human mammal”. 《Biochem Biophys Res Commun》 366 (1): 206–211. doi:10.1016/j.bbrc.2007.11.127. hdl:10069/22710. PMID 18054325.
- ↑ Hacein-Bey-Abina, S; Garrigue, A; Wang, GP; Soulier, J; Lim, A; Morillon, E; Clappier, E; Caccavelli, L; Delabesse, E; Beldjord, K; Asnafi, V; MacIntyre, E; Dal Cortivo, L; Radford, I; Brousse, N; Sigaux, F; Moshous, D; Hauer, J; Borkhardt, A; Belohradsky, BH; Wintergerst, U; Velez, MC; Leiva, L; Sorensen, R; Wulffraat, N; Blanche, S; Bushman, FD; Fischer, A; Cavazzana-Calvo, M (September 2008). “Insertional oncogenesis in 4 patients after retrovirus-mediated gene therapy of SCID-X1.”. 《The Journal of Clinical Investigation》 118 (9): 3132–42. doi:10.1172/JCI35700. PMC 2496963. PMID 18688285.
- ↑ Wang XG, Revskaya E, Bryan RA, Strickler HD, Burk RD, Casadevall A, Dadachova E (Oct 2007). “Treating cancer as an infectious disease-viral antigens as novel targets for treatment and potential prevention of tumors of viral etiology”. 《PLOS ONE》 2 (10): e1114. Bibcode:2007PLoSO...2.1114W. doi:10.1371/journal.pone.0001114. PMC 2040508. PMID 17971877.
- ↑ Molho-Pessach V, Lotem M (2007). 《Viral carcinogenesis in skin cancer》. 《Curr Probl Dermatol》. Current Problems in Dermatology 35. 39–51쪽. doi:10.1159/000106409. ISBN 978-3-8055-8313-8. PMID 17641489.
- ↑ Carrillo-Infante C, Abbadessa G, Bagella L, Giordano A (Jun 2007). “Viral infections as a cause of cancer (review)”. 《Int J Oncol》 30 (6): 1521–8. doi:10.3892/ijo.30.6.1521. PMID 17487374.
- ↑ 가 나 Blankson JN, Persaud D, Siliciano RF (2002). “The challenge of viral reservoirs in HIV-1 infection”. 《Annu. Rev. Med.》 53: 557–93. doi:10.1146/annurev.med.53.082901.104024. PMID 11818490.
- ↑ Finzi D, Hermankova M, Pierson T, 외. (November 1997). “Identification of a reservoir for HIV-1 in patients on highly active antiretroviral therapy”. 《Science》 278 (5341): 1295–300. Bibcode:1997Sci...278.1295F. doi:10.1126/science.278.5341.1295. PMID 9360927.
- ↑ Persaud D, Pierson T, Ruff C, 외. (April 2000). “A stable latent reservoir for HIV-1 in resting CD4(+) T lymphocytes in infected children”. 《J. Clin. Invest.》 105 (7): 995–1003. doi:10.1172/JCI9006. PMC 377486. PMID 10749578.
- ↑ Chun TW, Fauci AS (September 1999). “Latent reservoirs of HIV: obstacles to the eradication of virus”. 《Proc. Natl. Acad. Sci. U.S.A.》 96 (20): 10958–61. Bibcode:1999PNAS...9610958C. doi:10.1073/pnas.96.20.10958. PMC 34225. PMID 10500107.