이트라코나졸
이트라코나졸(Itraconazole, ITZ)은 여러 가지 진균 감염을 치료하는 데 사용되는 항진균제이다.[1] 적응증인 진균증에는 아스페르길루스증, 분아균증, 콕시디오이데스진균증, 히스토플라스마증, 파라콕시디오이데스진균증 등이 있다.[1] 경구 또는 정맥으로 투여할 수 있다.[1]
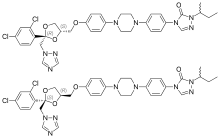
| |
| 체계적 명칭 (IUPAC 명명법) | |
|---|---|
| (±)-1-[(RS)-sec-butyl]-4-[p-[4-[p-[[(2R,4S)-rel-2-(2,4-dichlorophenyl)-2-(1H-1,2,4-triazol-1-ylmethyl)-1,3-dioxolan-4-yl]methoxy]phenyl]-1-piperazinyl]phenyl]-Δ2-1,2,4-triazolin-5-one | |
| 식별 정보 | |
| CAS 등록번호 | 84625-61-6 |
| ATC 코드 | J02AC02 |
| PubChem | 55283 |
| 드러그뱅크 | DB01167 |
| ChemSpider | 49927 |
| 화학적 성질 | |
| 화학식 | C35H38Cl2N8O4 |
| 분자량 | 705.64 |
| SMILES | eMolecules & PubChem |
| 약동학 정보 | |
| 생체적합성 | ~55%, 식사와 함께 투여 시 최대 |
| 단백질 결합 | 99.8% |
| 동등생물의약품 | ? |
| 약물 대사 | 간에서 대사 (CYP3A4) |
| 생물학적 반감기 | 21시간 |
| 배출 | 소변 (35%), 대변 (54%) |
| 처방 주의사항 | |
| 허가 정보 | |
| 임부투여안전성 | B3(오스트레일리아) C(미국) |
| 법적 상태 | |
| 투여 방법 | 경구(캡슐, 용액), 정맥(IV), 국소투여 |
일반적인 부작용으로는 메스꺼움, 설사, 복통, 발진, 두통이 있다.[1] 발생할 수도 있는 심각한 부작용에는 간 문제, 심부전, 스티븐스-존슨 증후군, 아나필락시스를 포함한 알레르기 반응이 있다.[1] 임신 중 또는 수유 중 사용이 안전한지 여부는 불분명하다. 트리아졸 계열의 약물에 속한다.[1] 진균의 세포막이나 신진대사에 영향을 주어 성장을 막는다.[1]
이트라코나졸은 1978년에 특허를 받았고 1992년에 미국에서 의료용으로 승인되었다.[1][2] 현재 WHO 필수 의약품 목록에 등재되어 있다.[3]
최근 연구에서는 이트라코나졸(ITZ)이 소니데깁(sonidegib)과 유사한 방식으로 헤지호그 경로(hedgehog pathway)[4]를 억제함으로써 암 치료에 사용될 수 있다고 주장한다.
의료용 편집
이트라코나졸은 플루코나졸보다 활성 스펙트럼이 더 넓으나 보리코나졸이나 포사코나졸만큼 넓지는 않다. 특히, 플루코나졸이 효과적이지 않은 아스페르길루스에 대해 효과적이다. 또한 분아균증(blastomycosis), 스포로트리쿰증(sporotrichosis), 히스토플라스마증(histoplasmosis), 손발톱진균증(onychomycosis)에 대해 사용이 허가되었다. 이트라코나졸은 99% 이상 단백질과 결합된 상태로 있으며 뇌척수액에 거의 침투하지 않는다. 따라서 수막염이나 기타 중추신경계 감염을 치료하는 데 사용해서는 안된다.[5] 존스홉킨스 가이드(Johns Hopkins Abx Guide)에 따르면 미미한 뇌척수액(CSF) 침투가 있지만 크립토코커스 및 콕시디오이데스 수막염에 대한 치료는 성공적이었다.[6]
또한 다른 항진균제가 부적절하거나 효과가 없는 아스페르길루스증, 칸디다증, 크립토콕쿠스증과 같은 전신 감염에도 처방된다.
지난 10년 동안 이트라코나졸은 기저세포암, 비소세포폐암, 전립선암 환자를 위한 항암제로 연구되었다.[7] 예를 들어, 진행성 전립선암 남성을 대상으로 한 2상 연구에서 고용량 이트라코나졸(600mg/day)은 유의한 PSA 반응 및 종양 진행 지연과 관련이 있었다. 이트라코나졸은 또한 화학요법제인 페메트렉세드(pemetrexed)와 병용했을 때 비소세포폐암 남성을 대상으로 한 2상 시험에서 활성을 보였다.[8][9][10] 최근 검토에서는 외과적으로 치료할 수 없는 진행성 및 전이성 기저 세포 암종에 대해 다른 화학요법제와 함께 국소 및 경구 사용을 강조했다.[11]
사용 가능한 제형 편집
이트라코나졸은 청색 22 밀리미터 (0.87 in) 로 생산된다. 작은 1.5 밀리미터 (0.059 in) 캡슐 내부에 파란색 알약이 있다. 각 캡슐에는 100 mg이 포함되어 있으며, 일반적으로 12시간 간격으로 하루에 두 번 복용한다. 이트라코나졸 스포라녹스(Sporanox) 브랜드는 존슨앤드존슨(Johnson & Johnson)의 자회사인 얀센제약(Janssen Pharmaceutica)에서 개발 및 판매하고 있다. 이 파란색 캡슐의 3층 구조로 되어 있는데 이트라코나졸이 불용성이며 pH에 민감하기 때문이다. 복잡한 제조공정을 위해 전문 기계가 필요할 뿐만 아니라 제조상의 어려움도 많다. 또한 알약이 상당히 커서 많은 환자들이 삼키기 어렵다. 스포라녹스를 만드는 과정의 일부는 대한민국 공개특허공보 제10-2001-2590호에 의해 밝혀졌다.[12] 캡슐에 들어있는 작은 파란색 알약은 벨기에 비어스(Beerse)에서 제조된다.[12][13]
약은 경구 용액이 더 잘 흡수된다. 경구용 용액에 포함된 사이클로덱스트린은 삼투성 설사를 유발할 수 있으며, 이것이 문제가 될 경우 용량의 절반은 경구용액으로, 절반은 캡슐제로 투여하여 사이클로덱스트린의 투여량을 줄일 수 있다. "스포라녹스" 이트라코나졸 캡슐은 흡수를 향상시키기 때문에 항상 음식과 함께 복용해야 하지만 "로자녹" 제조업체는 "식사와 관계없이" 복용할 수 있다고 주장한다.[14] 이트라코나졸 경구 용액은 식전 1시간 또는 식후 2시간에 복용해야 한다. 이는캡슐과 경구 용액을 함께 사용하는 경우에도 마찬가지이다. 이트라코나졸은 산에 의해 흡수가 개선되기 때문에 오렌지 주스나 콜라와 함께 복용할 수 있다. 제산제, H2 차단제, 양성자 펌프 억제제와 함께 복용하면 이트라코나졸의 흡수가 저해된다.
부작용 편집
이트라코나졸은 비교적 내약성이 좋은 약물이며(플루코나졸 또는 보리코나졸만큼 내약성이 낮지는 않지만) 그것이 생성하는 부작용의 범위는 다른 아졸계 항진균제와 유사하다.[15]
- 알라닌아미노전이효소 수치 증가는 이트라코나졸을 복용하는 사람들의 4%에서 발견된다.
- 울혈성 심부전 발병의 "사소하지만 실질적인 위험"[15]
- 간부전, 때로는 치명적일 수 있음
시럽 제조에 사용되는 사이클로덱스트린은 설사를 유발할 수 있다. 더 큰 문제를 나타낼 수 있는 부작용은 다음과 같다.
상호작용 편집
다음 약물은 이트라코나졸과 함께 복용해서는 안 된다.[16]
약리학 편집
약력학 편집
이트라코나졸의 작용 기전은 다른 아졸계 항진균제와 동일하다. 즉, 라노스테롤 14α-탈메틸화 효소 억제를 통해 에르고스테롤의 곰팡이 매개 합성을 억제한다. 시토크롬 P450 3A4 CC-3를 억제하는 능력 때문에 다른 약물과의 상호 작용을 고려할 때 주의해야 한다.[17]
이트라코나졸은 헤지호그 신호전달 경로(hedgehog signaling pathway)[18][19]와 혈관신생을 모두 억제하는 것으로 나타난 이 계열의 유일한 억제제라는 점에서 다른 아졸계 항진균제와 약리학적으로 구별된다.[20][21] 이러한 뚜렷한 활동은 시토크롬 P450 라노스테롤 14 알파 데메틸라제의 억제와 관련이 없으며 책임이 있는 정확한 분자 표적은 확인되지 않은 채로 남아 있다. 기능적으로 이트라코나졸의 항혈관신생 활성은 글리코실화, VEGFR 2 인산화,[21] 트래피킹,[22] 콜레스테롤 생합성 경로의 억제와 관련이 있는 것으로 나타났다.[20] 증거에 따르면 이트라코나졸에 의한 헤지호그 신호 전달의 억제에 대한 구조적 결정인자는 항혈관신생 활성과 관련된 것과 확연히 다르다.[23]
약동학 편집
사이클로스포린, 퀴니딘, 클래리스로마이신과 함께 이트라코나졸은 P-당단백질을 억제하여 유기 양이온 약물의 제거를 줄이고 흡수를 증가시켜 약물 상호작용을 일으킬 수 있다. 기존의 이트라코나졸 제제를 사용하면 혈청 농도가 환자마다 크게 달라질 수 있으며, 이로 인해 종종 치료 지수보다 혈청 농도가 낮아질 수 있다.[24] 따라서 환자는 식사 전보다는 지방이 많은 식사 후에 이트라코나졸을 복용하는 것이 일반적으로 권고되었다.[25][26]
유럽 연합의 분산 절차[27]를 통해 허가된 제품(Lozanoc)은 생체 이용률이 증가하고 식품의 동시 섭취에 대한 민감성이 감소하여 혈청 수준의 변동성이 감소했다.
화학 편집
이트라코나졸 분자는 3개의 키랄 탄소를 가지고 있다. 디옥솔란 고리의 두 키랄 중심은 서로에 대해 고정되어 있고, 트리아졸로메틸렌 및 아릴옥시메틸렌 디옥솔란-고리 치환기는 항상 서로에 대해 시스(cis)이다. 임상 제형은 4개의 입체 이성질체(2개의 거울상 이성질체 쌍)의 1:1:1:1 혼합물이다.[28][29]
역사 편집
이트라코나졸은 1992년 미국에서 의료용으로 승인되었다.[30]
참고 문헌 편집
미국 식품의약국(FDA)과 유럽의약청 (EMA)에 의해 희귀의약품으로 지정됐다.[31][32][33][34][35]
각주 편집
- ↑ 가 나 다 라 마 바 사 아 “Itraconazole”. The American Society of Health-System Pharmacists. 2017년 12월 8일에 확인함.
- ↑ Fischer, Jnos; Ganellin, C. Robin (2006). 《Analogue-based Drug Discovery》 (영어). John Wiley & Sons. 503쪽. ISBN 9783527607495.
- ↑ 《World Health Organization model list of essential medicines: 21st list 2019》. Geneva: World Health Organization. 2019. WHO/MVP/EMP/IAU/2019.06. License: CC BY-NC-SA 3.0 IGO.
- ↑ Li, Ke; Fang, Dengyang; Xiong, Zuming; Luo, Runlan (2019). “
Inhibition of the hedgehog pathway for the treatment of cancer using Itraconazole
”. 《OncoTargets and Therapy》 12: 6875–6886. doi:10.2147/OTT.S223119. ISSN 1178-6930. PMC 6711563. PMID 31692536. - ↑ Gilbert DN, Moellering, RC, Eliopoulos GM, Sande MA (2006). 《The Sanford Guide to antimicrobial therapy》. ISBN 978-1-930808-30-0.
- ↑ Pham, P; Bartlett, JG (2007년 7월 24일). “Itraconazole”. Johns Hopkins. 2007년 11월 28일에 원본 문서에서 보존된 문서.
- ↑ “Search results for Itraconazole”. 《ClinicalTrials.gov》. U.S. National Institutes of Health.
- ↑ “Itraconazole inhibits angiogenesis and tumor growth in non-small cell lung cancer”. 《Cancer Research》 71 (21): 6764–6772. 2011. doi:10.1158/0008-5472.CAN-11-0691. PMC 3206167. PMID 21896639.
- ↑ “Repurposing itraconazole as a treatment for advanced prostate cancer: a noncomparative randomized phase II trial in men with metastatic castration-resistant prostate cancer”. 《The Oncologist》 18 (2): 163–173. 2013. doi:10.1634/theoncologist.2012-314. PMC 3579600. PMID 23340005.
- ↑ “Phase 2 study of pemetrexed and itraconazole as second-line therapy for metastatic nonsquamous non-small-cell lung cancer”. 《Journal of Thoracic Oncology》 8 (5): 619–623. May 2013. doi:10.1097/JTO.0b013e31828c3950. PMC 3636564. PMID 23546045.
- ↑ “Itraconazole in the treatment of basal cell carcinoma: A case-based review of the literature”. 《Australasian Journal of Dermatology》 62 (3): 394–397. 2021. doi:10.1111/ajd.13655. PMID 34160824.
- ↑ 가 나 Composition comprising Itraconazole for oral administration Archived 2007년 2월 26일 - 웨이백 머신. 2004.
- ↑ Sporanox (Itraconazole Capsules) 보관됨 2008-07-05 - 웨이백 머신.
- ↑ “SUBA Bioavailability Technology”. Mayne Pharma Group.
- ↑ 가 나 “The Safety of Sporanox Capsules and Lamisil Tablets for the Treatment of Onychomycosis”. FDA Public Health Advisory. 2001년 5월 9일. 2009년 5월 28일에 원본 문서에서 보존된 문서. 2006년 8월 10일에 확인함.
- ↑ “Sporanox (Itraconazole) Capsules”. 《Safety Labeling Changes Approved By FDA Center for Drug Evaluation and Research》. U.S. Food and Drug Administration (FDA). 2016년 10월 26일에 원본 문서에서 보존된 문서. 2019년 12월 16일에 확인함.
- ↑ Katzung & Trevor's (2015). 《Pharmacology Examination & Board Review》. McGraw Hill. 397쪽.
- ↑ “Itraconazole, a Commonly Used Antifungal that Inhibits Hedgehog Pathway Activity and Cancer Growth”. 《Cancer Cell》 17 (4): 388–99. 2010. doi:10.1016/j.ccr.2010.02.027. PMC 4039177. PMID 20385363.
- ↑ “Itraconazole and arsenic trioxide inhibit hedgehog pathway activation and tumor growth associated with acquired resistance to smoothened antagonists”. 《Cancer Cell》 23 (1): 23–34. 2013. doi:10.1016/j.ccr.2012.11.017. PMC 3548977. PMID 23291299.
- ↑ 가 나 “Inhibition of Angiogenesis by the Antifungal Drug Itraconazole”. 《ACS Chemical Biology》 2 (4): 263–70. 2007. doi:10.1021/cb600362d. PMID 17432820.
- ↑ 가 나 “Itraconazole Inhibits Angiogenesis and Tumor Growth in Non-Small Cell Lung Cancer”. 《Cancer Research》 71 (21): 6764–72. 2011. doi:10.1158/0008-5472.CAN-11-0691. PMC 3206167. PMID 21896639.
- ↑ “Cholesterol trafficking is required for mTOR activation in endothelial cells”. 《Proceedings of the National Academy of Sciences》 107 (10): 4764–9. 2010. Bibcode:2010PNAS..107.4764X. doi:10.1073/pnas.0910872107. PMC 2842052. PMID 20176935.
- ↑ “Itraconazole Side Chain Analogues: Structure–Activity Relationship Studies for Inhibition of Endothelial Cell Proliferation, Vascular Endothelial Growth Factor Receptor 2 (VEGFR2) Glycosylation, and Hedgehog Signaling”. 《Journal of Medicinal Chemistry》 54 (20): 7363–74. 2011. doi:10.1021/jm200944b. PMC 3307530. PMID 21936514.
- ↑ “Systemic availability of itraconazole in lung transplantation”. 《Antimicrob. Agents Chemother.》 40 (9): 2217–20. 1996. doi:10.1128/AAC.40.9.2217. PMC 163504. PMID 8878612.
- ↑ “[Influence of foods on the absorption of antimicrobial agents]”. 《Nutr Hosp》 (스페인어) 12 (6): 277–88. 1997. PMID 9477653.
- ↑ “Food interaction and steady-state pharmacokinetics of itraconazole capsules in healthy male volunteers”. 《Antimicrob. Agents Chemother.》 37 (4): 778–84. 1993. doi:10.1128/aac.37.4.778. PMC 187759. PMID 8388198.
- ↑ “Lozanoc 50 Mg Hard Capsules (Itraconazole)” (PDF). 《Public Assessment Report Decentralised Procedure》. UK Medicines and Health Care Products Regulatory Agency.
- ↑ Kunze, KL; Nelson, WL; Kharasch, ED; Thummel, KE; Isoherranen, N (April 2006). “Stereochemical Aspects of Itraconazole Metabolism in vitro and in vivo”. 《Drug Metabolism and Disposition》 34 (4): 583–90. doi:10.1124/dmd.105.008508. PMID 16415110.
- ↑ “Itraconazole on Drugs.com”. 《Drugs.com》. 2016년 8월 28일에 확인함.
- ↑ “Itraconazole: FDA-Approved Drugs”. 《U.S. Food and Drug Administration (FDA)》. 2020년 5월 15일에 확인함.
- ↑ “Itraconazole Orphan Drug Designation”. 《U.S. Food and Drug Administration (FDA)》. 2016년 5월 19일. 2020년 5월 15일에 확인함.
- ↑ “Itraconazole Orphan Drug Designation”. 《U.S. Food and Drug Administration (FDA)》. 2016년 8월 16일. 2020년 5월 15일에 확인함.
- ↑ “Itraconazole Orphan Drug Designation”. 《U.S. Food and Drug Administration (FDA)》. 2008년 10월 30일. 2020년 5월 15일에 확인함.
- ↑ “EU/3/17/1901”. 《European Medicines Agency (EMA)》. 2017년 8월 23일. 2020년 5월 15일에 확인함.
- ↑ “EU/3/18/2024”. 《European Medicines Agency (EMA)》. 2018년 5월 25일. 2020년 5월 15일에 확인함.