NMDA 수용체
NMDA 수용체(영어: NMDA receptor, NMDAR)는 신경 세포에서 발견되는 글루탐산 수용체(Glutamate receptor) 및 이온 통로 단백질(Ion channel protein)이다. NMDA 수용체는 이온성 글루탐산 수용체의 세 가지 유형 중 하나이며, 나머지는, AMPA와 카인산 수용체(Kainate receptor)가 있다. 글루타메이트와 글리신이 결합할 때 활성화되며, 활성화되면 양으로 하전된 이온이 세포막을 통해 흐르면서 칼슘에 의한 세포신호(Cell signaling) 및 시냅스가소성(Synaptic plasticity) 조절, 기억세포 활성화에 관여한다.[2]
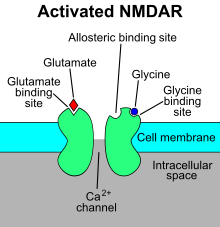
명칭은 N-메틸-D 아스파르트산염(N-methyl-D-aspartate, NMDA)에 선택적으로 결합하기 때문에 NMDA 수용체라고 명명되었다. 시냅스전(Presynapse)에서 글루탐산계 신경전달물질이 시냅스틈(Synaptic cleft)으로 유입되고, 시냅스틈에 유입된 글루탐산이 시냅스후 막에 존재하는 글루탐산 수용체와 결합하면 신경전달이 일어나는데, NMDA 수용체는 이 시냅스후 막에 존재하는 글루탐산 수용체의 일종인 것이다. NMDA 수용체는 마그네슘(Mg2+) 또는 아연(Zn2+)과 결합할 경우 양이온 통과성 잃기 때문에 탈분극 상태에서 마그네슘과 아연이 떨어져 나온 후에 비로소 제기능을 할 수 있다. NMDA 수용체는 나트륨(Na+)과 칼슘(Ca2+)을 신경세포 안에 들어올 수 있게 하며, 칼륨을 신경세포 밖으로 나가게 하는 이온 통로로 기능한다.[3]
역사 편집
NMDA 수용체 발견은 1960년대 NMDA 합성 연구에 참가한 제프 와킨스(Jeff Warkins) 일군의 과학자들에 의해 진행됐다. 1980년대 초에는 NMDA 수용체가 여러 중심 시냅스 경로에 관여하는 것으로 밝혀졌다.[4] 1990년대 초에는 신경회로의 소단위체에 대한 선택적 결합 여부가 밝혀졌는데, 대표적으로 신경회로 내 소단위체의 일종인 GluN2B에 대한 선택적 결합, 이를 통한 억제 공식의 성립이 이에 속한다.[5] 이후에는 간질, 파킨슨병, 알츠하이머, CNS 장애 들과 같은 다양한 신경계 장애에 관여한다는 사실도 밝혀지게 되었다.[6]
구조 편집
NMDA 수용체는 구조적으로 단백질 영역(Protein domain), 막횡단 영역(Transmembrane domain), 세포질 영역(Cytoplasmic domain)으로 나눠진다.
단백질 영역 편집
시냅스후 막 외부에 있는 글루탐산, 글리신 등의 리간드와 결합할 수 있는 영역이다. 이 영역은 NMDA 수용체가 특정한 기능을 하는 수용체로서 역할을 할 수 있게 한다.
막횡단 영역 편집
막횡단 영역은 시냅스후 막을 통과하는 형태의 단백질 영역이다. 구조는 하나의 막횡단나선을 갖는 일자원통형, 세 개의 막횡단나선을 갖는 교차형, 베타배열 구조를 가진 입체나선형이 존재한다. 소단위체 운반 등을 담당한다.
세포질 영역 편집
세포질 영역은 시냅스후 막 안쪽에 있는 영역으로, NMDA 수용체는 세포질 영역을 통하여 인산화효소와 결합하여 세포신호 조절에 직접적으로 관여한다.
결합 편집
NMDA 수용체에는 GluN1, GluN2, GluN3의 단백질 소단위체(Protein subunit)가 결합한다. GluN2는 GluN2A, GluN2B, GluN2C, GluN2D로 나눠지며, GluN3은 GluN3A, GluN3B로 나눠진다. 따라서 총 일곱 종류의 GluN 소단위체가 존재한다. 이 각각의 GluN은 각자의 GRIN을 형성한다. 하나의 NMDA 수용체에는 이 중 네 가지의 소단위체와 합성하여 사중합체 형태의 형성되는데, 이 사중합체 형성을 위해서는 필수적으로 두 개의 GluN1 소단위체가 결합되어야 한다. 즉, 일곱 종류가 자유롭게 포함될 수 있는 소단위체 결합 부위기는 두 개의 자리가 있다고 할 수 있다. 이 조합에 따라 NMDA 수용체가 갖는 특성이 결정된다.[7]
작용제 편집
작용제(agonist)는 세포내 수용체와 결합하여 해당 수용체를 활성화시켜 생물학적인 반응을 유도하는 물질을 의미한다. 작용제는 NMDA 수용체의 활성화에 직접적으로 관여하는 것으로, 이 개념을 다룰 때 빼놓을 수 없는 것이다.
NMDA 수용체의 활성화는 글루탐산 또는 아스파르트산염과의 결합을 필요로 하는데 이 과정의 효율성을 높이기 위해 작용제가 관여할 수 있다. 또한, 작용제는 이온 통로의 효과적인 개방을 유도하기도 한다. D-Serine의 경우는 글리신보다 더 효과적으로 NMDA 수용체의 작용력을 높이는 것으로 밝혀졌다. 동시에 D-Serine 형성 차단을 통하여 NMDA 수용체의 기능을 차단하여 매개 흥분성 신경 전달을 차단할 수도 있다.
길항제로 Remacemide가 있으며 이것은 NMDA 수용체의 비경쟁적 저해제이다. 글루타민 독성이 신경세포에 작용하는 것을 막는다.[8]
각주 편집
- ↑ Laube B, Hirai H, Sturgess M, Betz H, Kuhse J (March 1997). “Molecular determinants of agonist discrimination by NMDA receptor subunits: analysis of the glutamate binding site on the NR2B subunit”. 《Neuron》 18 (3): 493–503. doi:10.1016/S0896-6273(00)81249-0. PMID 9115742.
Since two molecules of glutamate and glycine each are thought to be required for channel activation (3, 6), this implies that the NMDA receptor should be composed of at least four subunits.
- ↑ Furukawa H, Singh SK, Mancusso R, Gouaux E (November 2005). "Subunit arrangement and function in NMDA receptors". Nature. 438 (7065): 185–92.
- ↑ Liu Y, Zhang J (October 2000). "Recent development in NMDA receptors". Chinese Medical Journal. 113 (10): 948–56.
- ↑ Yamakura T, Shimoji K (October 1999). "Subunit- and site-specific pharmacology of the NMDA receptor channel". Progress in Neurobiology. 59 (3): 279–98.
- ↑ Paoletti P, Neyton J (February 2007). "NMDA receptor subunits: function and pharmacology" Current Opinion in Pharmacology. 7 (1): 39–47.
- ↑ Dingledine R, Borges K, Bowie D, Traynelis SF (March 1999). "The glutamate receptor ion channels". Pharmacological Reviews. 51 (1): 7–61.
- ↑ Ryan TJ, Grant SG (October 2009). "The origin and evolution of synapses". Nature Reviews. Neuroscience. 10 (11): 701–12.
- ↑ Wolosker H (October 2006). ["D-serine regulation of NMDA receptor activity". https://www.semanticscholar.org/paper/D-serine-regulation-of-NMDA-receptor-activity.-Wolosker/5bb25f10a2077493d13ba981166f33145a4eeb6e] Science's STKE. 2006 (356): pe41