공유 결정
원자들의 공유 결합으로 형성된 결정 구조
공유 결정(共有結晶) 또는 공유 결합 결정은 전자를 내놓기 어려운 비금속 원소 사이에서 두 원자가 서로 전자를 내놓아 전자 쌍을 만들어 서로 공유하여 이루어진, 즉 공유 결합을 통해 형성된 결정이다. 대표적인 예시로 다이아몬드, 질화 붕소, 탄화 규소 등이 있다.[1][2]

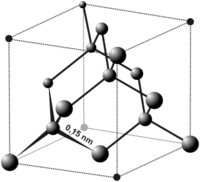
기본 구성 단위는 원자이며, 화학식으로 표기할 때는 구성 비율로 나타낸다.[3] 결정에는 금속 결정, 소금을 비롯한 이온 결정 및 분자 결합 결정 그리고 공유 결합 결정이 포함된다.[4] 공유 결합 결정와 공유 결합 결정의 한 형태인 유기 공유 골격체는 금속 결정 및 금속 유기 골격체보다 원자간의 인력이 강하게 작용한다.[5] 이온 결합으로 생성된 결정은 쉽게 부스러지지만, 공유 결합 결정은 원자간의 강한 인력이 작용하므로 쉽게 떨어지지 않는다. 따라서 공유결합결정 고체의 녹는점은 높은 편이며 잘 용해되지 않는다.[6] 극성 용매보다는 무극성 용매에 잘 녹는 경향이 있다. 액체일 경우 끓는점이 높다.[7]
대부분 이온이 없기에 전기가 통하지 않는다.[3] 공유 결합으로 형성되는 결정은 대부분 낮은 전도성을 가진다. 공유 결합 결정의 한 종류인 실리콘은 온도의 변화에 따라 컨덕턴스가 변화한다. 순수한 실리콘의 경우 낮은 온도에서는 전도성을 띄고 있지 않으나 온도에 따라 전도성이 변화하는 점 때문에 반도체의 재료로 사용된다.[8] 또한 흑연은 네 번째 전자가 평면상에서 자유롭게 움직일 수 있어 전류가 흐르는 것이 가능하다.[9]
각주
편집- ↑ “covalent crystal” (영어). doi:10.1093/oi/authority.20110803095644102. 2022년 5월 6일에 확인함.
- ↑ “공유결합결정”. 《두산백과》. 2022년 5월 6일에 확인함.
- ↑ 가 나 “공유 결정(covalent crystal)”. 《과학문화포털 사이언스올》. 2022년 5월 6일에 확인함.
- ↑ Michael 2013, General categories can be distinguished based on the nature of the building blocks and the bonding between them: metallic crystals, ionic crystals (the best-known example is perhaps sodium chloride), covalent crystals (such as diamond) and molecular crystals.
- ↑ Michael 2013, This means that the majority of MOFs are chemically and thermally less robust than covalent crystals such as diamond or zeolites
- ↑ “Covalent Crystals”. 《Introduction to Chemistry》. 2022년 5월 6일에 확인함.
- ↑ “Covalent crystals, Definition, Example, and Properties - Chemist Notes” (미국 영어). 2022년 5월 6일에 확인함.
- ↑ Dinesh 2020, Silicon's electrical conductivity increases with higher temperatures. Pure silicon has too low a conductivity (i.e., too high a resistivity) to be used as a circuit element in electronics.
- ↑ Chung, D. D. L. (2002년 4월 1일). “Review Graphite”. 《Journal of Materials Science》 (영어) 37 (8): 1475–1489. doi:10.1023/A:1014915307738. ISSN 1573-4803.
참고 자료
편집- Michael Mastalerz (2013년 9월 23일). “Covalent crystal growth”. 《Nature Chemistry》. (구독 필요).
- Dinesh Kumar; Mohit Johari (2020년 5월 5일). “Characteristics of silicon crystal, its covalent bonding and their structure, electrical properties, uses”. 《AIP Conference Proceedings》 2220 (1). (구독 필요).
| 이 글은 화학에 관한 토막글입니다. 여러분의 지식으로 알차게 문서를 완성해 갑시다. |