단백질 접힘
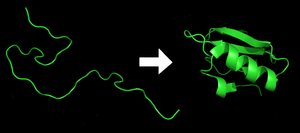
단백질 접힘(영어: protein folding)은 선형의 아미노산 복합체인 단백질이 개개의 단백질에 맞게 고유하게 정확히 접힌 구조를 형성하거나 안정화된 구조를 형성하는 과정을 말한다. 여기서 네이티브 폴딩(native folding)의 의미는 에너지 손실을 최저로 유지하면서 최적화에 도달하는 것을 가리킨다. 이러한 접힘에서의 고유한 형태는 고유한 기능의 결정과 매우 관련이 깊다.
발견
편집단백질의 화학적인 구조는 아미노산의 선형 복합체이다. 하지만, 대부분의 경우 단백질은 단순히 선형의 사슬 구조로 존재하지 않고 개개의 단백질에서 고유하게 접힌 형태로 존재한다. 20세기 중반에 미국의 화학자 안핀센(Anfinsen)은 리보뉴클레이스 A라는 단백질의 접힌 구조를 인위적으로 망가뜨린 다음, 적절한 조건에서 망가진 단백질이 다시 초기의 접힌 상태를 회복하는 것을 실험적으로 보여, 단백질의 아미노산 서열 자체의 정보가 고유한 접힌 형태를 결정한다는 것을 밝혔다. 안핀센은 이러한 업적으로 노벨 화학상을 수상하였다.[1] 안핀센의 연구 결과는 단백질 접힘을 결정하는 화학적 원리를 이해한다면 단백질의 아미노산 서열로부터 그 단백질의 고유한 접힌 구조를 예측할 수 있다는 것을 보여주었다.
단백질 접힘 문제
편집단백질의 아미노산 서열이 어떻게 고유한 접힌 구조를 결정하는지에 대한 질문을 단백질 접힘 문제라고 한다. 이 문제를 해결하기 위해 지난 수십여 년 동안 단백질 접힘을 결정하는 생화학적 원리를 이해하려는 노력이 꾸준히 이루어져 왔다. 초기에는 단백질 접힘의 가역적 성질을 이용하여, 단백질 구조를 인위적으로 풀거나 다시 접히도록 하여 그 화학 반응의 특성들을 주로 연구하였다. 1980년대에 들어 단백질 공학의 연구방법론이 적용되기 시작했다. 유전자 조작을 통해 단백질의 특정 아미노산을 다른 아미노산으로 바꾸었을 때의 변화가 어떤 영향을 주는지를 연구하면서 단백질 접힘에 대한 연구가 급진전을 이루게 되었다.
또한, 단백질 접힘 문제를 이론적으로 접근하여 실험이 제공하지 못하는 정보들을 얻으려는 노력도 계속되었다. 중요한 질문으로는 어떤 화학적 결합력이 최종 구조를 결정하는지, 반응 속도가 어떻게 결정되는지, 반응 중간생성물이 존재하는지, 반응 경로가 유일한지 아니면 다양한지 등이다. 수많은 연구 결과를 통하여 상당량의 정보가 축적되고 이 현상에 대한 이해가 깊어졌지만, 단백질 접힘 문제는 아직도 해결된 질문보다 더 많은 의문점을 남기고 있다.
단백질 접힘 문제의 궁극적인 해답은 주어진 아미노산 서열만으로 단백질의 접힌 구조를 예측할 수 있을 때 얻어진다고 볼 수 있다. 이러한 단백질의 구조 예측은 생화학 분야에서 가장 어려운 문제로 손꼽고 있다. 최근에는 생화학은 물론 이론화학, 물리학, 전산과학, 정보이론 등의 다양한 학문 분야에서 이 문제를 다루고 있고, 이러한 학제간 연구를 통하여 빠른 속도로 진전을 이루고 있다. 하지만 아직도 이 문제에 대한 해결은 단지 부분적으로만(크기가 작고 전형적인 구조를 가진 단백질에 한해서만) 제시되고 있을 뿐이다.
2021년 7월 ALPHAFOLD라는 딥 러닝 기반의 단백질 접합 구조예측 프로그램이 공개되었다. 이 프로그램은 CASP(Critical Assessment of protein Structure Prediction)에서 상당히 유효하다고 보여지는 결과에서 주목할만한 예측 프로그램으로 인정받았다.
또한 이러한 단백질 접힘 문제는 미스폴딩(misfolding, 잘못접힘)과도 관련이 있다. 여러 연구결과는 미스폴딩이 퇴행성 뇌질환 등과 같은 주요한 생명공학의 의문점들을 이해하는데 많은 정보를 제공하였다. 잘못접힘)은 언폴딩(unfolding)을 통해 다시 리폴딩(re-folding)되는 방향 또는 세포 수준에서 이를 분해하여 제거하는 방향이 확인되고 있다.
단백질 접힘의 기능
편집단백질 접힘은 단백질 분자를 구성하는 펩타이드 사슬 고유의 2차 구조의 배치 순서로 공간적 배치를 바꾸어 고차 구조를 형성하는 일이라고 전제할 때, 예를 들어 효소와 같은 경우 이러한 고유한 입체적 형태(3차원적 구조)에서 구현된 활성 부위을 통해 보다 온전하게 제 기능을 발휘하여 기질과의 결합을 성공적으로 이룰 수 있다. 한편 이러한 단백질 접힘의 기능에 따른 단백질의 분류는 효소, 조절 단백질, 운반 단백질, 구조 단백질 등이 있다.
같이 보기
편집각주
편집- ↑ “Press Release: The 1972 Nobel Prize in Chemistry” (영어). Nobelprize.org. 2012년 6월 23일에 확인함.
외부 링크
편집- (영어) Folding @ Home Archived 2008년 6월 16일 - 웨이백 머신
- (영어) Rosetta @ Home