팔면체형 분자기하
팔면체형 분자기하(八面體形分子幾何, 영어: octahedral molecular geometry)는 화학에서 6개의 배위자가 중심원자의 주위에 대칭적으로 배치되어, 그것이 정팔면체의 각정점을 형성하는 분자기하이다. 팔면체형 분자는 일반적으로 그 배위자 사이의 결합은 없다. 완전한 정팔면체는 군점 Oh에 속하고, 팔면체형 분자에는 육불화황과 몰리브덴헥사카르보닐 따위가 있다.
| 팔면체형 분자기하 | |
|---|---|
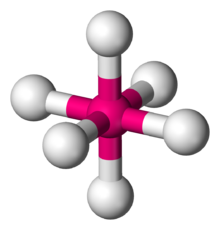 | |
| 예 | SF6, Mo(CO)6 |
| 점군 | Oh |
| 입체수 | 6 |
| 배위수 | 6 |
| 결합각 | 90° |
| μ (극성) | 0 |

팔면체형 배위기하 개념은 배위화합물의 화학양론과 화학이성(異性)을 설명하기 위해 알프레트 베르너가 개척했다. 그의 고찰에 따라 배위화합물의 이성질체수가 합리적으로 허용되게 되었다. 아민이나 간단한 음이온을 포함하는 팔면체 전이금속 착화합물은 종종 베르너 착화합물과 연관지어진다.
팔면체 착화합물의 이성질체
편집2종 또는 그 이상의 배위자 종류가 팔면체의 중심금속에 배위함에 따라 이성질체가 발생한다. 그들 이성질체의 명명(命名)은 다른 배위자끼리의 배치와 수에 의존한다.
cis와 trans
편집MLa4Lb2에는 2종의 이성질체가 존재한다. Lb가 서로 인접하고 있을 때 cis 형, Lb가 서로 180°의 위치관계에 있을 때 trans 형이다.
MLa2Lb2Lc2에서도 cis형과 trans형이 가능하다. La, Lb, Lc의 모든 배위자가 trans형인 경우와 단일 배위자만이 trans형이고 다른 두 배위자가 cis형인 경우가 있다.
facial과 meridional
편집MLa3Lb3에서는 같은 세 배위자가 서로 cis형인 facial형(fac)과, 같은 세 배위자가 동일평면 상에 있는 meridional형(mer )까지 2종의 이성질체가 가능하다.
-
cis -[CoCl2(NH3)4]+
-
trans -[CoCl2(NH3)4]+
-
fac -[CoCl3(NH3)3]
-
mer -[CoCl3(NH3)3]
카이랄성
편집두자리리간드를 2개 이상 갖는 착화합물에는 카이랄성이 발생한다. 3회 회전축에서 보면, 두자리 리간드가 형성되는 나선구조가 왼쪽으로 도는 것은 Λ(람다), 오른쪽으로 도는 것은 Δ(델타)체라고 부른다.
-
Λ-[Fe(ox)3]3−
-
Δ-[Fe(ox)3]3−
-
Λ- cis -[CoCl2(en)2]+
-
Δ- cis -[CoCl2(en)2]+
기타
편집가능한 이성질체의 수는 팔면체 착화합물의 배위자 종류가 모두 다를 때에 최대 30개이다. 다음 표는 한자리리간드의 조합에 따른 가능한 모든 이성질체의 수를 나타낸다.
| 화학식 | 이성질체의 수 | 거울상 이성질체의 수 |
|---|---|---|
| ML6 | 1 | 0 |
| MLa5Lb | 1 | 0 |
| MLa4Lb2 | 2 | 0 |
| MLa3Lb3 | 2 | 0 |
| MLa4LbLc | 2 | 0 |
| MLa3Lb2Lc | 3 | 0 |
| MLa2Lb2Lc2 | 6 | 1 |
| MLa3LbLcLd | 5 | 1 |
| MLa2Lb2LcLd | 8 | 2 |
| MLa2LbLcLdLe | 15 | 6 |
| MLaLbLcLdLeLf | 30 | 15 |
이 때, MLaLbLcLdLeLf의 15개 부분입체 이성질체는 모두 카이랄임에 비해, MLa2LbLcLdLe의 부분입체 이성질체의 6개는 카이랄이지만 La가 trans형일 때의 3종류는 그러하지 않다. 이러한 사실에서, 팔면체형 분자기하는 유기화학을 지배하는 사면체형 분자기하보다 훨씬 복잡하다는 것을 알 수 있다. 사면체형 분자 MLaLbLcLd에서는 거울상 이성질체는 한 쌍밖에 없으며, 유기화학에서 2개의 부분입체 이성질체를 만들어내려면 두 개의 부제탄소(不齊炭素)가 필요된다.