내재성 막 단백질
내재성 막 단백질(integral membrane protein)은 생물학적 막에 영구적으로 부착되는 막 단백질의 한 유형이다. 모든 막관통 단백질은 내재성 막 단백질이지만 모든 내재성 막 단백질이 막관통 단백질인 것은 아니다.[1] 내재성 막 단백질은 유기체의 게놈에 암호화된 단백질의 상당 부분을 구성한다.[2] 막을 가로지르는 단백질은 고리형 지질로 둘러싸여 있으며, 이는 막 단백질과 직접 접촉하는 지질로 정의된다. 이러한 단백질은 세제, 비극성 용매 또는 때로는 변성제를 사용하여 막에서 분리할 수 있다.
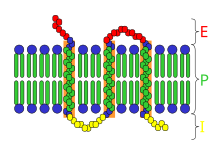
구조
편집~160개의 서로 다른 통합 막 단백질의 3차원 구조가 X선 결정학 또는 핵 자기 공명 분광학에 의해 원자 분해능에서 결정되었다. 그들은 추출 및 결정화와 관련된 어려움으로 인해 연구에 도전적인 주제이다. 또한 내재성 막 단백질의 많은 수용성 단백질 도메인의 구조는 Protein Data Bank에서 확인할 수 있다. 추출 및 결정화를 용이하게 하기 위해 멤브레인 고정 α-나선이 제거되었다.
내재성 막 단백질은 두 그룹으로 나눌 수 있다.
- 통합 폴리토프 단백질(Transmembrane protein)
- 통합 모노토프 단백질
통합 폴리토프 단백질
편집내재성 막 단백질의 가장 일반적인 유형은 전체 생체막에 걸쳐 있는 막횡단 단백질 (TM)이다. 단일 통과 막 단백질은 막을 한 번만 통과하는 반면, 다중 통과 막 단백질은 여러 번 교차하면서 안팎으로 엮인다. 단일 패스 TM 단백질은 카복실 말단이 세포질을 향하도록 위치하는 유형 I 또는 아미노 말단이 세포질을 향하도록 위치하는 유형 II로 분류될 수 있다. 유형 III 단백질은 단일 폴리펩타이드에 다중 막횡단 도메인을 갖는 반면 유형 IV는 막을 통해 채널에서 함께 조립된 여러 상이한 폴리펩타이드로 구성된다. 유형 V 단백질은 공유 연결된 지질을 통해 지질 이중층에 고정된다. 마지막으로 유형 VI 단백질은 막횡단 도메인과 지질 앵커를 모두 가지고 있다.[3]
통합 모노토프 단백질
편집통합 모노토프 단백질(Integral monotopic protein)은 한쪽에서 막과 연결되어 있지만 지질 이중층에 완전히 걸쳐 있지는 않다.
단백질 구조의 결정
편집NIH(National Institutes of Health)의 일부인 미국 국립 일반 의학 연구소 NIGMS)가 자금을 지원하는 PSI(rotein Structure Initiative)는 막 단백질을 포함하여 구조 생물학에서 3차원 단백질 구조를 결정하고 사용 기술을 개발하는 것을 목표로 한다. 상동성 모델링은 아미노산 서열과 관련된 상동성 단백질의 실험적 3차원 구조로부터 "표적" 통합 단백질의 원자 분해능 모델을 구성하는 데 사용할 수 있다. 이 절차는 리간드 -G 단백질 결합 수용체 (GPCR) 및 그 복합체에 광범위하게 사용되었다.[4]
기능
편집내재성 막 단백질에는 수송체, 링커, 채널, 수용체, 효소, 구조적 막 고정 도메인, 에너지 축적 및 변환에 관여하는 단백질, 세포 부착을 담당하는 단백질이 포함된다. 운송업자의 분류는 운송업자 분류 데이터베이스에서 찾을 수 있다.[5]
내재성 막 단백질(이 경우 세균성 광포착 색소, 박테리오로돕신)와 인지질 이중층에 의해 형성된 막 사이의 관계의 예는 다음과 같다. 이 경우 통합 막 단백질은 인지질 이중층에 7번 걸쳐 있다. 이중층의 소수성 영역에 포함된 단백질 부분은 알파 나선이며 주로 소수성 아미노산으로 구성된다. 단백질의 C 말단 말단은 세포질에 있고 N 말단 영역은 세포 외부에 있다. 이 특정 단백질을 포함하는 막은 광합성에서 기능할 수 있다.[6]
예시
편집통합 막 단백질의 예시는 다음과 같다.
- 인슐린 수용체
- 인테그린, 카드 헤린, NCAM 또는 셀렉틴과 같은 일부 유형의 세포 접착 단백질 또는 세포 접착 분자(CAM)
- 일부 유형의 수용체 단백질
- 글리코포린(glycophorin)
- 로돕신
- 밴드 3(band 3)
- CD36
- 포도당 투과효소
- 이온 채널 및 게이트
- 갭 접합 단백질
- G 단백질 결합 수용체 (예: 베타-아드레날린성 수용체)
- 세이핀(seipin)
같이 보기
편집각주
편집- ↑ Steven R. Goodman (2008). 《Medical cell biology》. Academic Press. 37–쪽. ISBN 978-0-12-370458-0. 2010년 11월 24일에 확인함.
- ↑ “Genome-wide analysis of integral membrane proteins from eubacterial, archaean, and eukaryotic organisms”. 《Protein Science》 7 (4): 1029–38. 1998. doi:10.1002/pro.5560070420. PMC 2143985. PMID 9568909.
- ↑ Nelson, D. L., & Cox, M. M. (2008). Principles of Biochemistry (5th ed., p. 377). New York, NY: W.H. Freeman and Company.
- ↑ “Structural model of ligand-G protein-coupled receptor (GPCR) complex based on experimental double mutant cycle data: MT7 snake toxin bound to dimeric hM1 muscarinic receptor.”. 《J Biol Chem》 286 (36): 31661–75. September 2011. doi:10.1074/jbc.M111.261404. PMC 3173127. PMID 21685390.
- ↑ “The Transporter Classification Database: recent advances”. 《Nucleic Acids Res.》 37 (Database issue): D274–8. January 2009. doi:10.1093/nar/gkn862. PMC 2686586. PMID 19022853.
- ↑ “Integral membrane proteins”. 《academic.brooklyn.cuny.edu》. 2015년 2월 1일에 원본 문서에서 보존된 문서. 2015년 1월 29일에 확인함.