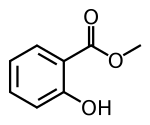
살리실산 메틸
화합물
살리실산메틸(Methyl salicylate)은 살리실산의 에스테르화 반응에 의해 생성된 살리실산메틸은 소염 - 진통제로 이용되고, 아세틸살리실산(아스피린)은 진통 - 해열제로 이용된다. 살리실산메틸과 아세틸살리실산은 모두 진통 작용을 하지만, 가수 분해가 일어날 경우 살리실산메틸은 인체에 해로운 메탄올이 생성되므로 먹는 약으로는 이용하지 않는다.
| |||
| |||

| |||
| 이름 | |||
|---|---|---|---|
| IUPAC 이름
Methyl 2-hydroxybenzoate
| |||
별칭
| |||
| 식별자 | |||
3D 모델 (JSmol)
|
|||
| ChEBI | |||
| ChEMBL | |||
| ChemSpider | |||
| ECHA InfoCard | 100.003.925 | ||
| EC 번호 |
| ||
| KEGG | |||
PubChem CID
|
|||
| RTECS 번호 |
| ||
| UNII | |||
CompTox Dashboard (EPA)
|
|||
| |||
| |||
| 성질 | |||
| C8H8O3 | |||
| 몰 질량 | 152.149 g·mol−1 | ||
| 겉보기 | Colorless liquid | ||
| 냄새 | sweet, rooty | ||
| 밀도 | 1.174 g/cm3 | ||
| 녹는점 | −8.6 °C (16.5 °F; 264.5 K) | ||
| 끓는점 | 222 °C (432 °F; 495 K) [1] Decomposes at 340–350 °C[2] | ||
| 0.639 g/L (21 °C) 0.697 g/L (30 °C)[2] | |||
| 용해도 | Miscible in organic solvents | ||
| acetone에서의 용해도 | 10.1 g/g (30 °C)[2] | ||
| 증기 압력 | 1 mmHg (54 °C)[1] | ||
| 산성도 (pKa) | 9.8[3] | ||
자화율 (χ)
|
−8.630×10−5 cm3/mol | ||
굴절률 (nD)
|
1.538 | ||
| 위험 | |||
| 주요 위험 | Harmful | ||
| GHS 그림문자 |  [1] [1]
| ||
| 신호어 | 경고 | ||
| H302[1] | |||
| P264, P270, P280, P301+312, P302+352, P305+351+338, P321, P330, P332+313, P337+313, P362, P501 | |||
| NFPA 704 (파이어 다이아몬드) | |||
| 인화점 | 96 °C (205 °F; 369 K) [1] | ||
| 452.7 °C (846.9 °F; 725.8 K)[1] | |||
달리 명시된 경우를 제외하면, 표준상태(25 °C [77 °F], 100 kPa)에서 물질의 정보가 제공됨.
| |||
각주
편집- ↑ 가 나 다 라 마 바 Sigma-Aldrich Co. Retrieved on 2013-05-23.
- ↑ 가 나 다 “Methyl salicylate”. 《chemister.ru》.
- ↑ Scully, F. E.; Hoigné, J. (January 1987). “Rate constants for reactions of singlet oxygen with phenols and other compounds in water”. 《Chemosphere》 16 (4): 681–694. Bibcode:1987Chmsp..16..681S. doi:10.1016/0045-6535(87)90004-X.
외부 링크
편집- 위키미디어 공용에 살리실산 메틸 관련 미디어 분류가 있습니다.


