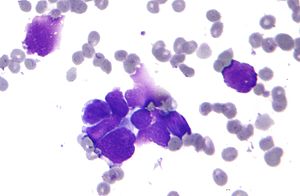
소세포암종
소세폼암종은 매우 악성적인 암인데 다른 신체, 예들 들어 자궁경관[1]이나 전립선[2] , 위장관 등에서도 발생할 수도 있지만 대부분은 폐에서 발생한다.[3] 비소세포암종과 비교했을 때, 소세포암종은 짧은 분열 기간과 높은 성장률을 보이며 폐전이로 빠르게 발전된다. 확장기에서의 소세포 폐암은 흔하지 않은 장애이다.[4] 10년간의 관련 생존율 (한정적 소세포암과 확장적 소세포암 모두 포함)은 3.5% (여성은 4.3%, 남성은 2.8%)이다.[5]
 | |
|---|---|
| 다른 이름 | 소세포폐암 |
 | |
| 진료과 | 종양학 |
소세포암 종류
편집소세포암은 두 가지의 임상병리학적인 단계, 제한기(LS)와 확장기(ES)로 분리된다.[6] 일반적으로 종양이 흉곽에 한정되어있는지 여부, 흉부의 종양이 실제로 단순한 방사선 치료로 가능한지, 폐전이의 유무로 단계을 결정을 짓는다.[7] 일반적으로 종양이 한쪽 폐에만 있고 림프절이 그 폐에 가깝다면, 암은 제한기라고 불린다. 그 이상을 넘는다면 ES라고 불린다.
제한기-소세포암
편집제한기에서는 병용화학요법(주로 시스플라틴이나 카보플라틴, 에토포시드)이 현재 흉부 방사선치료과 함께 사용된다.[8][9][10] 방사선 치료는 제한기-소세포암에서 생존율을 높여주는 것으로 보여준다.
확장기-소세포암
편집이 문단은 아직 미완성입니다. 여러분의 지식으로 알차게 문서를 완성해 갑시다. |
확장기에서는, 백금계의 화학요법이 치료의 기준
증상과 징후
편집소세포암은 보통 중앙부 호흡기에 존재하고 점막하조직에 침투하여 기관지 기도를 좁힌다. 흔한 증상은 기침, 호흡곤란, 체중감소 그리고 쇠약 등이 있다. 소세포암 환자의 70% 이상이 전이상 질환을 보이는데 공통적으로 간, 부신, 뼈, 뇌 등으로 전이된다. 높은 수준의 신경내분비의 특성으로 인하여, 소세포암은 부신피질자극호르몬(ACTH)와 항이뇨호르몬(ADH)을 포함한 이소성 호르몬을 만든다. 많은 양의 항이뇨호르몬은 항이뇨호르몬 분비이상 증후군(SIADH)을 일으킨다. 램버트-이튼 근무력증 증후군(LEMS)은 소세포암과 관련된 잘 알려진 방종양성(paraneoplastic) 증상이다.[11]
소세포 폐암
편집페이터 세포라고 불리는 기관지의 신경내분비 세포 (APUD 세포)로부터 유래된다고 여겨진다. 그래서 그들은 신경내분비 표지를 만들고 방종양성 증후군이나 쿠싱 증후군을 가지고 오는 항이뇨호르몬이나 부신피질자극호르몬과 같은 이성 호르몬의 생성을 이끈다.
폐암은 세계적으로 남성과 여성 사이에 가장 높은 사망률을 보이는 암사망의 주요인이다. 때로는 납작한 세포 모양과 듬성한 세포질로 인하여 "연맥세포암"이라고 부른다. 소세포암을 진단할 때 특히 주의가 요구되는데, 소세포 종피종이 ㅡ매우 희귀한 폐암의 아류형ㅡ 소세포암으로 오인될 수 있기 때문이다.
램버트-이튼 증후군(LEMS)으로 진단된 절반 이상이 결국 소세포암으로 발견된다.
소세포 암종은 비소세포폐암보다 훨씬 넓고 빨리 전이가 된다.[12] (단계별로 조금씩은 다름) 그리고 보통 폐문과 종격 림프절의 초기 침투가 동반된다.[13] 전이 과정의 메카니즘은 잘 알려져 있지 않다.
c-SCLC
편집소세포 암종은 특히 악성 조직 합성물을 포함한 다양한 다른 조직변이들 과의 결합으로 발생한다. 한 개 이상의 개별화된 폐암의 형태가 발견되면, 예를 들어 편평세포암종이나 선암종과 같은, 악성 종양으로 진단되고 결합된 소세포암종으로 분류된다. (c-SCLC). 결합 소세포 암종은 현재 소세포암종의 아류로 분류된다.
비록 현재 결합소세포암의 병기중에 있고 단독의 소세포암과 동일하게 치료받고 있음에도, 최근 연구는 종양 극초기엔 수술로 나은 결과를 만들 수 있다고 주장하고 있다. 흡연은 중요하고 위험한 요소이다. 증상과 징후는 다른 폐암과 비슷하다. 게다가, 신경내분비세포의 기원때문에, 소세포암은 램버트-이튼 무신경증 증후군과 같은 반신증후군을 초래하는 물질을 발생시킨다.
폐외 소세포암
편집매우 드물게 소세포암의 주된 발원지는 폐의 외부에 있거나 흉막에 존재한다. 이럴 경우, 폐외 소세포암이라고 명해진다(EPSCC). 호흡기 외부에 있는 소세포암은 전립선, 간, 췌장, 위장관, 방광에 나타날 수 있다. 미국에서는 일년에 1,000가지의 새로운 케이스가 보고된다. 조직학적으로 소세포암과 비슷하여, 소세포암 치료는 보통 폐외 소세포암을 치료하는데 사용된다. 1차 치료는 시스플라틴과 에토포사이드를 주로 사용한다. 일본에서는 1차치료제로 이리노테칸과 시스플라틴을 사용하는 것으로 옮겨지고 있다. 주된 부위가 피부일 경우, 메르켈 세포암이라고 불린다.
림프절에 제한된 폐외 소세포암종
편집소세포암중 특히 드물다. 과학계에서 존재하는 정보가 거의 없다. 오직, 한 두개의 림프절에서 발생되고 몸의 다른 부분엔 드물다. 소세포암과 치료는 동일하지만 생존률이 다른 소세포암보다는 높은 편이다.
전립선 소세포암
편집전립선 소세포암은 전립선 암중에서도 매우 희귀하다.(대략 1%) 전립선 특이 항원 수치의 변화가 거의 없기 때문에 전립선 소세포암은 전이 후의 말기에서 발견된다. 전립선 소세포암의 뇌전이는 매우 드물고, 나쁜 예후를 보인다.
유전학
편집TP53 유전자는 소세포암의 70-90프로에서 변이된다. RB1과 망막아종은 소세포암에서는 대부분 비활성화된다.
PTEN은 2~10%가 변이된다. MYC, MYC 계열의 구성성분의 증가가 소세포암의 30%에서 발견된다. 3번 염색체 이형접합의 손실은 소세포암 80%이상에서 발견되는데 종양억제 인자의 감소를 가지고 온다. 백개의 염색체 전좌가 계속해서 보고되고 있다(미텔만 데이터베이스,종양학과 혈액학의 유전학과 세포유전학의 아틀라스를 참고)
진단
편집- 국한 : 암은 폐안에 한정된다 (일명 : 소세포암 제한기
- 국소진행 : 암은 흉부안에 (소세포암 제한기 그리고 확장기 사이) 림프절(또는 샘)에 퍼져있다. 폐밖으로 이동하는 암세포를 수집하는 등, 림프절은 폐의 외부에서 정화하는 시스템으로써 작동한다.
- 원격전이 : 암은 신체의 다른 부분으로 전이되거나 퍼져있다 (일명 : 소세포암의 확장기)
진단시, 60~70%의 사람들은 이미 폐전이가 된다. 소세포암은 초창기 세포들로 구성된 미분화 종양이다. 이름에서 추측하 듯, 소세포암의 세포들은 일반적인 세포들 보다 작고, 세포질을 위한 어떤 공간이 거의 없다. 몇몇의 연구자들은 세포의 크기를 조절하는 메카니즘에 실패로 소세포암을 바라본다.
치료
편집소세포암은 한개의 약을 따로 쓰는 것보다 두가지 약을 혼용해서 치료하는 것이 훨씬 효과적이다.
화학요법
- 시스플라틴과 에토포시드
- 키보플라틴과 에토포시드
시스플라틴 내성
편집파클리탁셀은 시스플라틴 내성 암에 유용한 치료제이다. 파클리탁셀 저항세포의 66.7%, 시스플라틴 내성암의 68.1%는 파클리탁셀에 민감한 것으로 보인다. 이 활동의 메커니즘은 알려져 있지 않다. 파클리탁셀 기본의 화학요법은 적절한
면역치료
편집2018년, FDA는 소세포암과 관련되어 두가지 면역치료를 승인했다.
- 니볼루맙 (옵디보)
- 아테졸리주말(티센트릭)
자금논란
편집티센트릭 치료는 평균적으로 한달에 13,200달러가 든다. 최신 자료에 따르면 확장기 소세포암 환자의 30%이상이 화학치료만 할 경우보다, 24개월의 높은 생존율을 보임에도 불구하고, 캐나다 규제기관은 소세포암 확장기 환우를 위한 티센트릭 자금지원을 너무 비싸다는 이유로 거절해오고 있다. 영국 또한 약의 효율성을 언급하였다.
방사선치료
편집흉부 방사선은 암세포를 죽임으로써 SCLC 환자들이 좀 더 오래살 수 있게 도와주고 암 재발방지를 돕는다. 다른 종류의 방사선으로 예방 두 개 방사선은 중앙 신경 시스템의 재발을 방지하고, LD방사선과 ED화학요법에 완전한 결과와 매우 좋은 응답과 같은, 좋은 수행 성과로 환자들의 생존을 높이고 있다.
재발 케이스
편집만약 치료 후 소세포암이 발생된다면, 아래와 같은 약의 조합이 구제요법으로 유용할 것이다.
새로운 제제
편집테모졸로이드와 벤다무스틴을 포함한 몇개의 새로운 제제들이 재발한 소세포암에서 활동성을 갖는다. 특히 테모졸로마이드는 소세포암으로 인해 뇌전이에서 38%의 반응률을 보인다. 50명의 환자들의 임상실험에서 테모졸로마이드는 소세포암으로 인해 뇌전이된 38%의 반응률을 보이고, 무진행 생존율은 4.2개월이고 전반적인 생존율은 8.5개월이었다.
루르비니테딘은 민감한 질환자들 사이에서 재발된 소세포암의 전반적인 생존율을 상당히 높이는 유망한 새로운 제제이다. 단독 제제로서 루르비니테딘은 난치성 소세포암 임상실험에서 다음과 같은 결과를 증명했다.
- 민감한 질병인 15.2개월의 생존율 (화학요법 제거 90일 이상)은 질병 제한기에선 79.3% 전반적인 응답률에선 46.6%이다.
- 전반적인 5.1개월 생존율 (화학요법 제거 90일 미만)은 질병 제한기에선 46.8%, 전반적인 응답률에선 21.3%이다.
루르비니테딘은 랜덤화된 3단계에서 두번째 라인 치료에 있어 독소루비신과 결합되어 발견되는 중이다. 반면에 전반적인 생존율은 아직 알려지지 않았음에도, 두번째 라인에서의 생존율은 아래와 같다.
- 5.8개월의 중간 생존율을 가진 민감 질병에서의 생존율은 91.7%
- 3.5개월의 중간 생존율을 가진 저항 질병에서의 생존율은 33.3%
루르비니테딘은 현재 미국에서 EAP라는 프로그램아래 이용가능하다. CKD4/6D억제제인 트라일래시클립은 소세포암 치료를 위한 화학요법으로 인해 몸에 생긴 독성을 제거해준다. 트라일래시클립의 개발자인 G1 테라퓨틱스는 FDA가 신약 응용 프로그램을 고려하는 동안에 조금 더 확장된 접근안에서 트라일래시클립의 사용을 가능하게 한다.
신약응용확장프로그램(NDA)의 승인 결정은 2021년 2월 15일로 기대된다. 2021년 12월 2월, FDA가 브랜드 코셀라라는 화학요법으로 야기된 골수억제의 부작용 빈도를 줄이기 위한 치료제로서 트릴라씨클립을 승인하였다.
예후
편집확장기와 제한기를 포함해서 소세포암의 생존율을 여성은 3.6%~32.2%이고, 남성은 2.2~24.5%이다. 두 성의 상대적 생존율은 1975년 3.6%에서 2014년 6.7%로 증가했다. 소세포암은 화학요법과 방사선 요법에 민감하고 특히 백금에 기반을 둔 치료에도 민감하다. 그러나 이 질병을 가진 대다수 사람들은 재발하고 생존율을 매우 낮다. 지난 몇년간 미국에서 소세포암의 사망률과 발생률은 점점 줄어들고 있다.
5년이상의 장기적인 생존은 적절한 치료로 가능하다. 17세기 폐암과 관련된 세계 회의에 따르면, 대략 5주기의 화학치료와, 방사선 치료와 예방적 전두 방사선을 받은 환자들은 5년 이상의 중간 생존율을 보였다. 몇몇 케이스에서, 10년 이상의 장기 생존율은 화학요법과 방사선효과 각각 받음으로써 얻어지는 것을 보였다.
유럽 연구지 BMJ에 따르면, 화학요법에 면역요법을 적용하는 최근의 진보에도 불구하고, 폐암 아형중 최악의 종류는 중기 생존율이 대략 1년이었다. 이러한 열악한 결과와 싸우고자 제약 개발과 추가적인 시도에 대한 분명한 니즈가 있었다.
제한기에서, 상대적으로 5년간의 생존율(성, 인종, 나이)은 21.3%이다. 그러나 5년 생존율은 여성이 26.9%로 조금 더 높았다. 그리고 남자나 21.3%로 낮았다. 5년간 의 생존율을 보이는 소세포암의 확장단계에서는 예후가 훨씬 좋지 않다. 그러나 여성은 5년 생존율이 3.4% 높고, 남성은 2.2%로 낮은 생존율을 보인다.
5년간의 생존율
편집나이와, 성과 인종에 기반을 둔, 5년간의 관찰자가 트렉킹한 생존율은 가장 정확한 생존 정보라고 여겨진다. 이러한 데이터베이스는 소세포암의 다양한 단계를 묘사하기 위해 현지화, 지역화,그리고 떨어진것과 같은 용어를 쓴다.
모든 성과 인종에서 보인 5년간 생존율은 아래와 같다.
- "현지화" 소세포암 : 28.5%
- "지역화" 소세포암 : 14.9%
- "떨어진" 소세포암 : 2.9%
성에 의한 생존율
편집소세포암에 의해 영향을 받은 여성은 남성보다 5년이나 높은 생존율을 보인다.
- "현지화" : 여성 - 32.2% | 남성 -24.5%
- "지역화" : 여성 - 17% | 남성 -12.3%
- "떨어진" : 여성 - 3.6% | 남성 - 2.2%
인종, 성,나이에 의한 생존율
편집5년 간 상대적인 생존 통계는 좀 더 정확하고, 몇 개의 케이스는 특정 인종이나 연령대가 특정 진단을 받은 성과 합쳐진 것보다 높다. 예를 들어,
- 흑인/여성 | 나이 <50 (진단시) | 떨어진(소세포암 확장기) = 7.0%
- 백인/여성 | 나이 <50 (진단시) | 떨어진(소세포암 확장기)= 6.1%
국가 암 기관인 SEER는 특별한 생존율을 위해 공식적으로 오픈 가능한 데이터베이스를 유지한다.
역학
편집미국에서 15%의 폐암이 이런 타입이다. 소세포암은 흡연자에게서 나타나는데, 대부분 애연가에게 나타나고, 비흡연자들에게 드물다.
반항적 암연구법
편집2013년, 미국 의회는 반항적 연구법을 통과했다. 이것은 특히 소세포암을 포함한 다루기 어려운 암에 대한 관심을 불러일으켰다. 이것이, 컨소시엄을 통해 특정 연구를 진행하고, 소세포암을 지원하는 국립 암 연구소를 이끌었다. 결론적으로, 소세포암을 위한 새로운 실험약(ORY-1001과 키투르다 포함)이 현재 테스트 중이다.
같이 보기
편집각주
편집- ↑ Nasu K, Hirakawa T, Okamoto M, Nishida M, Kiyoshima C, Matsumoto H, 외. (March 2011). “Advanced small cell carcinoma of the uterine cervix treated by neoadjuvant chemotherapy with irinotecan and cisplatin followed by radical surgery”. 《Rare Tumors》 3 (1): 18–20. doi:10.4081/rt.2011.e6. PMC 3070456. PMID 21464879.
- ↑ Capizzello A, Peponi E, Simou N, Ntaskagiannis D, Tasiou I, Kamina S, Tsekeris P (February 2011). “Pure small cell carcinoma of the prostate: a case report and literature review”. 《Case Reports in Oncology》 4 (1): 88–95. doi:10.1159/000324717. PMC 3072185. PMID 21475596.
- ↑ "small-cell carcinoma" - 돌란드 의학사전
- ↑ “Small Cell Lung Cancer”. 《National Organization for Rare Disorders》.
- ↑ “Small cell carcinoma of the Lung and Bronchus”. 《Surveillance, Epidemiology, and End Results (SEER) Relative Survival Rates by Time Since Diagnosis》. U.S. National Cancer Institute. 2016.
- ↑ Chan BA, Coward JI (October 2013). “Chemotherapy advances in small-cell lung cancer”. 《Journal of Thoracic Disease》 5 (Suppl 5): S565–S578. doi:10.3978/j.issn.2072-1439.2013.07.43. PMC 3804877. PMID 24163749.
- ↑ Argiris A, Murren JR (2001). “Staging and clinical prognostic factors for small-cell lung cancer”. 《Cancer Journal》 7 (5): 437–447. PMID 11693903.
- ↑ “Limited-stage small cell lung cancer: Initial management”. 《www.uptodate.com》. UpToDate. 2019년 6월 2일에 확인함.
- ↑ “Small Cell Lung Cancer Treatment”. 《National Cancer Institute》. U.S.: National Cancer Institute, United States Department of Health and Human Services. 1980년 1월 1일. 2019년 6월 2일에 확인함.
- ↑ Sherman CA, Rocha Lima CM, Turrisi AT (October 2000). “Limited small-cell lung cancer: a potentially curable disease”. 《Oncology》 14 (10): 1395–403; discussion 1403–4, 1409. PMID 11098505. 2019년 2월 5일에 원본 문서에서 보존된 문서. 2021년 8월 1일에 확인함.
- ↑ Titulaer MJ, Verschuuren JJ (2008). “Lambert-Eaton myasthenic syndrome: tumor versus nontumor forms”. 《Annals of the New York Academy of Sciences》 1132 (1): 129–134. Bibcode:2008NYASA1132..129T. doi:10.1196/annals.1405.030. PMID 18567862. S2CID 22482871.
- ↑ Cotran, Ramzi S.; Kumar, Vinay; Fausto, Nelson; Nelso Fausto; Robbins, Stanley L.; Abbas, Abul K. (2005). 《Robbins and Cotran pathologic basis of disease》. St. Louis, Mo: Elsevier Saunders. 759쪽. ISBN 978-0-7216-0187-8.
- ↑ Mitchell, Richard Sheppard; Kumar, Vinay; Abbas, Abul K.; Fausto, Nelson (2007). 〈Ch. 13, box on morphology of small-cell lung carcinoma〉. 《Robbins Basic Pathology》 8판. Philadelphia: Saunders. ISBN 978-1-4160-2973-1.