사이안화 수소
화합물
(사이안화 수소산에서 넘어옴)
사이안화 수소(hydrogen cyanide) 혹은 청화수소(靑化水素), 청산(靑酸, prussic acid)은 화학식이 HCN인 화합물이다. 물, 에테르, 에탄올 등에는 반드시 녹으며, 거기서도 수용액은 별명이 사이안화 수소산 또는 청산이다. 무색인 맹독성 화합물이며, 휘발성이 있다. 치사량은 2g이며, 불에도 잘 탄다. 실온보다 약간 높은 26°C에서 끓는다. 쓴맛이며 아몬드향이 나지만 유전적 소인으로 냄새를 맡지 못하는 사람도 있다. 사이안화 수소는 약산이며 수용액에서 사이안화 음이온(CN–)을 내놓으며 부분적으로 이온화된다.
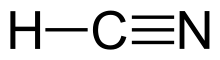
| |||
| |||
| 이름 | |||
|---|---|---|---|
| IUPAC 이름 | |||
별칭
| |||
| 식별자 | |||
3D 모델 (JSmol)
|
|||
| 3DMet | |||
| ChEBI | |||
| ChemSpider | |||
| ECHA InfoCard | 100.000.747 | ||
| EC 번호 |
| ||
| KEGG | |||
| MeSH | Hydrogen+Cyanide | ||
PubChem CID
|
|||
| RTECS 번호 |
| ||
| UNII | |||
| UN 번호 | 1051 | ||
CompTox Dashboard (EPA)
|
|||
| |||
| |||
| 성질 | |||
| HCN | |||
| 몰 질량 | 27.0253 g/mol | ||
| 겉보기 | Colorless liquid or gas | ||
| 냄새 | Oil of bitter almond | ||
| 밀도 | 0.6876 g cm−3[3] | ||
| 녹는점 | −13.29 °C (8.08 °F; 259.86 K)[3] | ||
| 끓는점 | 26 °C (79 °F; 299 K)[3] | ||
| Miscible | |||
| 에탄올에서의 용해도 | Miscible | ||
| 증기 압력 | 100 kPa (25 °C)[4] | ||
헨리 상수 (kH)
|
75 μmol Pa−1 kg−1 | ||
| 산성도 (pKa) | 9.21 (in water),
12.9 (in DMSO)[5] | ||
| 염기도 (pKb) | 4.79 (cyanide anion) | ||
| 짝산 | Hydrocyanonium | ||
| 짝염기 | Cyanide | ||
굴절률 (nD)
|
1.2675[6] | ||
| 점도 | 0.183 mPa·s (25 °C)[7] | ||
| 구조 | |||
| C∞v | |||
| Linear | |||
| 2.98 D | |||
| 열화학 | |||
열용량 (C)
|
35.9 J K−1 mol−1 (gas)[8] | ||
표준 몰 엔트로피 (S
|
201.8 J K−1 mol−1 | ||
표준 생성 엔탈피 (ΔfH⦵298)
|
135.1 kJ mol−1 | ||
| 위험 | |||
| GHS 그림문자 |    
| ||
| 신호어 | 위험 | ||
| H225, H300, H310, H319, H330, H336, H370, H400, H410 | |||
| P210, P261, P305+351+338 | |||
| NFPA 704 (파이어 다이아몬드) | |||
| 인화점 | −17.8 °C (0.0 °F; 255.3 K) | ||
| 538 °C (1,000 °F; 811 K) | |||
| 폭발 한계 | 5.6% – 40.0%[9] | ||
| 반수 치사량 또는 반수 치사농도 (LD, LC): | |||
LC50 (median concentration)
|
501 ppm (rat, 5 min) 323 ppm (mouse, 5 min) 275 ppm (rat, 15 min) 170 ppm (rat, 30 min) 160 ppm (rat, 30 min) 323 ppm (rat, 5 min)[10] | ||
LCLo (lowest published)
|
200 ppm (mammal, 5 min) 36 ppm (mammal, 2 hr) 107 ppm (human, 10 min) 759 ppm (rabbit, 1 min) 759 ppm (cat, 1 min) 357 ppm (human, 2 min) 179 ppm (human, 1 hr)[10] | ||
| NIOSH (미국 건강 노출 한계): | |||
PEL (허용)
|
TWA 10 ppm (11 mg/m3) [skin][9] | ||
REL (권장)
|
ST 4.7 ppm (5 mg/m3) [skin][9] | ||
IDLH (직접적 위험)
|
50 ppm[9] | ||
| 관련 화합물 | |||
관련 alkanenitriles
|
|||
달리 명시된 경우를 제외하면, 표준상태(25 °C [77 °F], 100 kPa)에서 물질의 정보가 제공됨.
| |||
제법
편집요즈음에는 사이안화 수소가 세가지 방법으로 대량으로 제조된다.
- CH4 + NH3 + 1.5O2 → HCN + 3H2O
반응에 필요한 에너지는 메테인과 암모니아의 산화에서 얻는다.
- CH4 + NH3 → HCN + 3H2
- CH(O)NH2 → HCN + H2O
실험실에서 소량의 사이안화 수소는 알칼리 금속과의 사이안화물에 산을 첨가해 만든다.
- H+ + NaCN → HCN + Na+
이 방법은 중독의 원인이 되기도 한다. 산이 비휘발성의 사이안화물을 사이안화 수소 기체로 바꾸기 때문이다.
각주
편집- ↑ “Hydrogen Cyanide – Compound Summary”. 《PubChem Compound》. United States: National Center for Biotechnology Information. 2004년 9월 16일. Identification. 2012년 6월 4일에 확인함.
- ↑ “hydrogen cyanide (CHEBI:18407)”. 《Chemical Entities of Biological Interest》. UK: European Bioinformatics Institute. 2009년 10월 18일. Main. 2012년 6월 4일에 확인함.
- ↑ 가 나 다 Haynes, 4.67
- ↑ Haynes, 6.94
- ↑ Evans, D. A. “pKa's of Inorganic and Oxo-Acids” (PDF). 2020년 6월 19일에 확인함.
- ↑ Patnaik, P. (2002). 《Handbook of Inorganic Chemicals》. McGraw-Hill. ISBN 978-0-07-049439-8.
- ↑ Haynes, 6.231
- ↑ Haynes, 5.19
- ↑ 가 나 다 라 NIOSH Pocket Guide to Chemical Hazards. “#0333”. 미국 국립 직업안전위생연구소 (NIOSH).
- ↑ 가 나 “Hydrogen cyanide”. 《Immediately Dangerous to Life and Health Concentrations (IDLH)》. National Institute for Occupational Safety and Health (NIOSH).
외부 링크
편집| 이 글은 화학에 관한 토막글입니다. 여러분의 지식으로 알차게 문서를 완성해 갑시다. |


