플라빈 아데닌 다이뉴클레오타이드
플라빈 아데닌 다이뉴클레오타이드(영어: flavin adenine dinucleotide, FAD)는 생화학에서 산화환원반응의 조효소이며, 보다 구체적으로 단백질의 보결분자단으로 물질대사에 있어서 몇 가지 중요한 효소 반응에 관여한다. 플라보단백질은 플라빈기를 함유하고 있는 단백질이며, 플라빈 아데닌 다이뉴클레오타이드(FAD) 또는 플라빈 모노뉴클레오타이드(FMN)의 형태일 수 있다. 석신산 탈수소효소 복합체의 구성 성분 외에도 α-케토글루타르산 탈수소효소 및 피루브산 탈수소효소 복합체의 구성 성분을 포함하는 많은 플라보단백질들이 있다.
| |
| 식별자 | |
|---|---|
3D 모델 (JSmol)
|
|
| 3DMet | |
| 1208946 | |
| ChEBI | |
| ChEMBL | |
| DrugBank | |
| ECHA InfoCard | 100.005.149 |
| EC 번호 |
|
| 108834 | |
| KEGG | |
| MeSH | Flavin-Adenine+Dinucleotide |
PubChem CID
|
|
| UNII | |
CompTox Dashboard (EPA)
|
|
| |
| |
| 성질 | |
| C27H33N9O15P2 | |
| 몰 질량 | 785.557 g·mol−1 |
| 겉보기 | White, vitreous crystals |
| log P | -1.336 |
| 산성도 (pKa) | 1.128 |
| 염기도 (pKb) | 12.8689 |
달리 명시된 경우를 제외하면, 표준상태(25 °C [77 °F], 100 kPa)에서 물질의 정보가 제공됨.
| |
FAD는 플라빈-N(5)-옥사이드, 퀴논, 세미퀴논, 하이드로퀴논의 4가지 서로 다른 산화환원상태로 존재할 수 있다.[1] FAD는 전자를 주거나 받아들임으로써 이들 상태들 사이에서 전환될 수 있다. FAD는 완전히 산화된 형태 또는 퀴논 형태에서 두 개의 전자와 두 개의 양성자를 받아서 FADH2(하이드로퀴논 형태)가 된다. 세미퀴논(FADH·)은 한 개의 전자와 한 개의 양성자를 각각 주거나 받아들임으로써 FADH2의 산화 또는 FAD의 환원에 의해 형성될 수 있다. 그러나 일부 단백질은 플라빈 보조 인자의 초과산화 형태인 플라빈-N(5)-옥사이드를 생성하고 유지한다.[2][3]
역사
편집플라보단백질은 1879년에 우유의 성분을 분리함으로써 처음 발견되었다. 처음에는 우유에서 기원했고, 노란색 색소였기 때문에 락토크롬(lactochrome)이라고 불렸다.[4] 과학계가 노란색 색소의 원인이 되는 분자를 확인하는 실질적인 진전을 이루는 데에는 50년이 걸렸다. 1930년대에는 많은 플라빈과 니코틴아마이드 유도체들의 구조가 발표되고, 산화환원반응의 촉매 작용에서 필수적인 역할을 하는 조효소에 대한 연구가 시작되었다. 독일의 과학자 오토 하인리히 바르부르크와 발터 크리스티안(Walter Christian)은 1932년에 세포 호흡에 필요한 효모에서 유래한 노란색 단백질을 발견했다. 그들의 동료인 후고 테오렐은 이 노란색 효소를 주효소()와 노란색 색소로 구분하고, 주효소만 또는 색소만으로는 NADH를 산화시킬 수 없었고, 주효소(apoenzyme)와 색소를 다시 섞으면 NADH를 산화시키는 효소 활성이 회복된다는 것을 보여주었다. 1937년에 테오렐은 이 색소가 효소의 보조 인자에 대한 최초의 직접적인 증거인 리보플라빈 인산 에스터인 플라빈 모노뉴클레오타이드(FMN)라는 것을 확인했다.[5] 1938년에 바르부르크와 크리스티안은 비슷한 실험을 통해 FAD가 D-아미노산 산화효소의 보조 인자라는 것을 발견했다.[6] 니코틴아마이드와 수소화물의 전달을 연결시키고 플라빈을 발견한 바르부르크의 연구는 1940년대와 1950년대에 많은 과학자들이 수많은 생화학에서의 산화환원반응들을 발견하고, 이들을 시트르산 회로와 ATP 합성과 같은 대사 경로에서 함께 연결시키는 길을 열었다.
특성
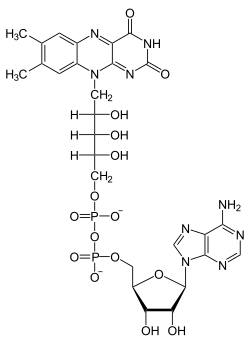
편집플라빈 아데닌 다이뉴클레오타이드(FAD)는 아데닌 뉴클레오타이드(아데노신 일인산, AMP)와 인산기를 통해 함께 결합된 플라빈 모노뉴클레오타이드(FMN)라는 두 가지 주요 부분으로 구성된다. 아데닌은 고리형 리보스의 1' 탄소에서 결합하고, 인산은 리보스의 5' 탄소에서 결합하여 아데닌 뉴클레오타이드를 형성한다. 리보플라빈은 아이소알록사진과 리비톨 사이의 탄소-질소(C-N) 결합에 의해 형성된다. 그 후에 인산기는 말단의 리비톨 탄소 상에 결합하여 FMN을 형성한다. 아이소알록사진과 리비톨 사이의 결합은 글리코사이드 결합으로 간주되지 않기 때문에 플라빈 모노뉴클레오타이드는 엄격한 의미로 뉴클레오타이드가 아니다.[7] 그래서 다이뉴클레오타이드라는 이름은 오해의 소지가 있지만, 플라빈 모노뉴클레오타이드는 구조 및 화학적 특성에서 여전히 뉴클레오타이드에 매우 가깝다.
FAD는 2 H+ 및 2 e−를 얻어서 FADH2로 환원될 수 있다. 또한 FADH2는 1 H+ 와 1 e−를 잃어 버려서 FADH로 산화될 수 있다. FADH가 1 H+ 와 1 e−를 추가로 소실하면 FAD로 산화될 수 있다. 또한 FAD의 형성은 플라빈-N(5)-옥사이드의 환원 및 탈수를 통해 일어날 수 있다.[8] 산화 상태에 기초하여 플라빈은 수용액에 있을 때 특정 색상을 취한다. 플라빈-N(5)-옥사이드(초과산화된)는 노란-오렌지색, FAD(완전히 산화된)는 노란색, FADH(반쯤 환원된)는 pH를 기준으로 파란색 또는 빨간색, 완전히 환원된 형태는 무색이다.[9][10] 산화환원 형태를 바꾸는 것은 다른 화학적 특성에 큰 영향을 미칠 수 있다. 예를 들어 완전히 산화된 형태인 FAD는 친핵성 공격의 대상이고, 완전히 환원된 형태인 FADH2는 높은 분극률을 가지고, 반쯤 환원된 형태는 수용액에서 불안정하다.[11] FAD는 방향족 고리 시스템이지만, FADH2는 그렇지 않다. 이것은 FADH2가 방향족 구조가 제공하는 공명을 통한 안정화 없이 에너지가 상당히 높다는 것을 의미한다. FADH2는 일단 산화되면 방향족성을 회복하고 이러한 안정화에 의해 나타나는 에너지를 방출하기 때문에 에너지 운반 분자이다.
FAD 및 그 변이체의 분광학적 특성은 자외선 가시광선 분광법 및 형광 분광법을 사용해 반응 모니터링을 수행해 조사할 수 있다. FAD의 각기 다른 형태는 흡광도 스펙트럼이 다르므로, 산화 상태의 변화를 쉽게 관찰할 수 있다.[11] FAD에 대한 주요 국소 흡광도는 최대치는 450 nm에서 관찰되었으며, 흡광 계수는 11,300 이었다.[12] 플라빈은 일반적으로 결합하지 않을 때 형광 활성을 갖는다(플라빈 핵산 유도체와 결합한 단백질을 플라보단백질이라 한다). 이러한 특성은 결합 상태에 놓였을 때 형광 활성의 소실을 관찰함으로써 단백질 결합 검사시 사용할 수 있다.[11] 산화된 플라빈은 약 450 nm의 높은 흡광도를 가지며, 약 515~520 nm에서 형광을 낸다.[9]
화학적 상태
편집생물체에서 완전히 산화된 형태인 FAD는 H− 및 e−의 수용체로, FADH는 수용체나 공여체로, 환원된 FADH2는 공여체로 작용한다. 아래의 도표는 일어날 수 있는 위치 에너지의 변화를 요약한 것이다.
위의 도표처럼 FAD의 다른 반응 형태들이 형성되고 소비될 수 있다. 이러한 반응들은 전자의 전달과 화학 결합의 생성/분해를 포함한다. 반응 메커니즘을 통해 FAD는 생물체 내에서의 화학 반응에 기여할 수 있다. 다음 그림들은 FAD가 관여할 수 있는 일부 반응들의 일반적인 형식을 보여준다.
메커니즘 1과 2는 하이드라이드를 얻는 것을 나타내며, 분자는 1개의 하이드라이드 이온에 해당하는 양을 얻는다. 메커니즘 3과 4는 라디칼의 형성 및 하이드라이드의 소실 과정이다. 라디칼은 전자쌍을 이루고 있지 않은 전자를 가진 원자를 포함하며, 화학적으로 반응성이 매우 크다. 하이드라이드의 소실은 이전의 하이드라이드를 얻는 과정의 역과정이다. 메커니즘 5와 6은 친핵성 첨가반응과 탄소 라디칼을 이용한 반응을 보여준다.
생합성
편집FAD는 리보플라빈에서 기원하는 또 다른 분자인 플라빈 모노뉴클레오타이드와 함께 효소 보조인자로서 중요한 역할을 한다.[8] 세균, 균류, 식물은 리보플라빈을 생성할 수 있지만, 사람과 같은 다른 진핵생물들은 리보플라빈을 만드는 능력을 상실했다.[9] 그러므로 사람은 비타민 B2로도 알려진 리보플라빈을 음식물에서 섭취해야 한다.[13] 리보플라빈은 일반적으로 소장에서 흡수되고, 운반 단백질을 통해 세포로 운반된다.[9] 리보플라빈 키네이스(EC 2.7.1.26)가 리보플라빈에 인산기를 추가하여 플라빈 모노뉴클레오타이드를 생성한 다음, FAD 합성효소가 아데닌 뉴클레오타이드를 부착시키는데 두 효소 모두 ATP를 필요로 한다.[9] 세균은 일반적으로 한 개의 이기능성 효소를 가지고 있지만, 고균과 진핵생물은 보통 2개의 다른 효소를 사용한다.[9] 최근의 연구는 세포기질과 미토콘드리아에 다른 아이소자임이 존재한다는 것을 보여준다.[9] FAD는 세포기질과 미토콘드리아에서 모두 합성되고 필요한 곳으로 운반될 수 있는 것으로 보인다.[11]
기능
편집플라보단백질의 산화환원 반응을 촉매하기 위해 플라빈 잔기의 독특하고, 다양한 구조를 이용한다. 플라빈은 여러 개의 산화환원 상태를 가지고 있기 때문에, 한 개 또는 두 개의 전자, 수소 원자 또는 하이드로늄 이온(H3O+)이 전달을 포함하는 과정에 참여할 수 있다. 또한 완전히 산화된 플라빈 고리의 N5와 C4a는 친핵성 공격을 받기 쉽다.[14] FAD 잔기의 이온화와 변형의 다양성은 아이소알록사진 고리 시스템과 플라빈 아데닌 다이뉴클레오타이드(FAD)를 포함하여 결합시 플라빈의 반응속도 매개변수를 크게 교란시키는 플라보단백질의 능력에 기인할 수 있다.
게놈(플라보프로테옴)에서 플라빈 의존성 단백질을 암호화하고 있는 유전자의 수는 생물 종에 따라 다르며, 0.1%~3.5%의 범위일 수 있으며, 사람은 90개의 플라보단백질을 암호화하고 있는 유전자를 가지고 있다.[15] FAD는 플라빈의 보다 복잡하고 풍부한 형태이며, 전체 플라보프로테옴의 75%[15] 및 사람에서 발현되는 플라보단백질들의 84%에 결합하는 것으로 보고되었다.[16] 포유류의 다양한 배양 세포주에서 유리 플라빈 또는 비공유결합 플라빈의 세포 내 농도가 FAD(2.2~17.0 amol/세포), FMN(0.46~3.4 amol/세포)로 보고되었다.[17]
FAD는 NAD+보다 더 플러스인 환원전위를 가지며, 매우 강력한 산화제이다. 세포는 C-C 결합을 알켄으로 탈수소화하는 것과 같은 에너지적으로 어려운 많은 산화반응에 이를 이용한다. FAD-의존성 단백질은 전자전달, DNA 복구, 뉴클레오타이드 생합성, 지방산의 베타 산화, 아미노산의 이화작용, CoA, CoQ, 헴기와 같은 보조 인자의 합성을 포함한 다양한 대사 경로에서 기능을 한다. 잘 알려진 반응 중 하나는 시트르산 회로의 일부이다. 석신산 탈수소효소(전자전달계의 복합체 II)는 유비퀴논을 유비퀴놀로 환원시키는 것과 석신산을 푸마르산으로 산화시키는 것을 짝지어 촉매하기 위해 효소에 공유결합된 FAD를 필요로 한다.[11] 이러한 산화로부터 나오는 고에너지 전자는 FAD를 FADH2로 환원시킴으로써 저장된다. FADH2는 전자전달계를 통해 두 개의 고에너지 전자를 전달하고 다시 FAD로 산화된다. FADH2의 에너지는 산화적 인산화에 의해 1.5 당량의 ATP를 생성하기에 충분하다.[18] 또한 지방산의 베타 산화 및 류신(아이소발레릴-CoA 탈수소효소), 아이소류신(짧은/가지사슬 아실-CoA 탈수소효소), 발린(아이소뷰티릴-CoA 탈수소효소), 리신(글루타릴-CoA 탈수소효소)과 같은 아미노산의 분해와 관련이 있는 아실-CoA 탈수소효소와 같이 FAD와 비공유결합을 하는 플라보단백질도 존재한다.[19] 물질대사를 조절하는 FAD-의존성 효소의 또 다른 예로는 글리세롤 3-인산 탈수소효소와 퓨린 뉴클레오타이드의 분해에 관여하는 잔틴 산화효소가 있다.[20] FAD의 다른 비촉매적 역할로는 플라보단백질에서 구조적 역할을 수행하거나, 생물 발광을 하는 세균에서 생체 시계, 성장, 빛의 발생을 조절하는 청색광 수용체와 관련된 역할도 있다.[19]
플라보단백질
편집플라보단백질은 보결분자단으로 FMN 또는 FAD를 가지고 있으며, 이러한 보결분자단은 단단히 묶여 있거나 공유 결합으로 연결될 수 있다. 플라보단백질의 약 5~10% 만이 FAD와 공유 결합으로 연결되어 있고, 이들 효소는 더 강력한 산화환원력을 가지고 있다.[11] 경우에 따라 FAD는 활성 부위에 대한 구조적 지지를 제공하거나 촉매 작용동안 중간생성물의 안정화를 제공할 수 있다.[19] 이용가능한 구조 데이터에 기초하여, 알려져 있는 FAD-결합 부위는 200개 이상의 서로 다른 유형으로 분류될 수 있다.[21]
사람에는 90 종의 플라보단백질이 있다. 이 중 약 84%는 FAD를 필요로 하고, 약 16%는 FMN을 필요로 하며, 5가지 단백질은 FAD와 FMN 둘 다를 필요로 한다.[16] 플라보단백질은 자신의 산화환원력 때문에 주로 미토콘드리아에 위치한다.[16] 전체 플라보단백질 중 90%는 산화환원반응을 수행하고(산화환원효소), 나머지 10%는 전이효소, 분해효소, 이성질화효소, 연결효소이다.[15]
탄소-헤테로 원자 결합의 산화
편집탄소-질소
편집모노아민 산화효소(MAO)는 노르에피네프린, 세로토닌, 도파민의 이화작용과 관련하여 생물학적으로 중요하기 때문에 광범위하게 연구된 플라보효소(flavoenzyme)이다. 모노아민 산화효소는 이민으로부터 알데하이드 또는 케톤으로 비효소적으로 가수분해함으로써 1차 아민, 2차 아민, 3차 아민을 산화시킨다. 비록 이러한 종류의 효소가 광범위하게 연구되었지만, 그 작용 메커니즘은 여전히 논쟁 중이다. 라디칼 메커니즘(radical mechanism)과 친핵성 메커니즘(nucleophilic mechanism)의 두 가지 메커니즘이 제안되었다. 라디칼 중간생성물의 존재를 나타내는 스펙트럼 또는 전자 스핀 공명에 대한 증거가 없기 때문에 라디칼 메커니즘은 일반적으로 잘 받아들여지지 않는다. 친핵성 메커니즘은 기질의 친핵성을 증가시킬 것으로 예상되는 2개의 티로신 잔기를 돌연변이시킨 부위 특이적 돌연변이 유발에 의해 지지되기 때문에 보다 더 선호된다.[22]
탄소-산소
편집글루코스 산화효소(GOX)는 효소 결합 플라빈의 환원과 함께 β-D-글루코스의 D-글루코노--δ-락톤으로의 산화를 촉매한다. 글루코스 산화효소는 각각의 소단위체가 하나의 FAD-분자와 결합하고 있는 호모다이머(homodimer)로 존재한다. 결정 구조는 FAD가 이량체 경계면 근처의 효소의 깊은 곳에 결합한다는 것을 보여준다. 연구에 따르면 FAD를 8-하이드록시-5-카바-5-데자 FAD(8-hydroxy-5-carba-5-deaza FAD)로 대체했을 때 반응의 입체화학은 플라빈의 전면과 반응하여 결정된다고 나왔다. 회전하는 동안 라디칼 메커니즘을 나타내는 중성 및 음이온 세미퀴논이 관찰된다.[22]
탄소-황
편집프레닐시스테인 분해효소(PCLase)는 단백질 표적에 아이소프레노이드 알데하이드와 유리된 시스테인 잔기를 형성하기 위해 프레닐시스테인(단백질 변형)의 분해를 촉매한다. FAD는 프레닐시스테인 분해효소에 비공유결합되어 있다. 플라빈의 반응을 보면 많은 메커니즘 연구가 이루어지지 않았지만, 제안된 메커니즘은 아래와 같다. 프레닐 잔기의 C1으로부터 FAD로의 하이드라이드의 전달은 플라빈의 FADH2로의 환원 및 이웃하는 황 원자에 의해 안정화된 탄소 양이온의 형성이 일어날 것으로 제안되었다. FADH2는 산화된 효소를 회복시키기 위해 산소 분자와 반응한다.[22]
탄소-탄소
편집UDP-N-아세틸에놀피루빌글루코사민 환원효소(MurB)는 에놀피루빌-UDP-N-아세틸글루코사민(기질)을 UDP-N-아세틸무람산(생성물)으로의 NADPH-의존성 환원을 촉매하는 효소이다. UDP-N-아세틸에놀피루빌글루코사민 환원효소는 단량체이며, FAD 한 분자를 포함하고 있다. 기질이 생성물로 전환되기 전에 NADPH는 먼저 FAD를 환원시켜야 한다. 일단 NADP+가 해리되면, 기질이 결합할 수 있고, 환원된 플라빈은 생성물을 환원시킬 수 있다.[22]
티올/이황화물 화학
편집글루타티온 환원효소(GR)는 글루타티온 이황화물(GSSG)을 글루타티온(GSH)으로의 환원을 촉매한다. 글루타티온 환원효소는 이 반응을 촉진시키기 위해 FAD와 NADPH를 필요로 한다. 먼저 하이드라이드를 NADPH에서 FAD로 전달해야 한다. 환원된 플라빈은 이황화물을 공격하기 위한 친핵체로써 작용할 수 있으며, 이는 C4a-시스테인 부가물을 생성한다. 이 부가물을 제거하면 플라빈-티올레이트 전하이동 복합체가 생성된다.[22]
전자전달 반응
편집마이크로솜의 P450 시스템의 환원효소인 사이토크롬 P450 환원효소에는 FMN과 FAD가 모두 포함되어 있다. 전자는 NADPH에서 사이토크롬 P450 환원효소의 FAD로 전달된 다음 FMN으로 전달되고, 마지막으로 사이토크롬 P450의 헴 보조인자로 전달된다. 환원 적정에서 FMN과 FAD는 모두 중성 세미퀴논으로 존재할 수 있는 것으로 밝혀졌다. 플라빈들은 단지 약 4Å 떨어져 있는데, 이는 전자가 그들 사이에서 직접적으로 전달된다는 것을 시사하고 있다.[22]
미토콘드리아 P450 시스템의 환원효소인 아드레노독신 환원효소는 효소의 FAD-결합 도메인에 박혀있는 FAD를 포함한다.[23] 아드레노독신 환원효소는 NADP-결합 도메인에서 NADPH와 결합한다. 아드레노독신 환원효소의 구조는 효율적인 전자전달을 위해 전자공여체인 NADPH와 전자수용체인 FAD의 정렬을 정확하게 유지하는 것으로 보아 확실하게 보존된다.[23]
마이크로솜의 환원효소의 구조와 미토콘드리아 P450 시스템의 환원효소의 구조는 완전히 다르며, 어떠한 상동성도 보이지 않는다.[24]
산화환원반응
편집p-하이드록시벤조에이트 하이드록실레이스(PHBH)는 p-하이드록시벤조에이트(pOHB)의 3,4-다이하이드록시벤조에이트(3,4-diOHB)로의 산소첨가 반응을 촉매한다. FAD, NADPH 및 산소 분자는 모두 산소첨가 반응에 필요하다. NADPH는 먼저 FAD로 하이드라이드를 전달하여 FADH−를 생성한 다음, NADP+는 효소로부터 분리된다. 환원된 p-하이드록시벤조에이트 하이드록실레이스는 산소 분자와 반응하여 플라빈-C(4a)-하이드로퍼옥사이드를 생성한다. 플라빈 하이드로퍼옥사이드는 p-하이드록시벤조에이트를 빠르게 하이드록실화 한 다음, 물을 제거하여 산화된 플라빈을 재생한다.[22] 대체 메커니즘인 플라빈 매개 산소 첨가 메커니즘은 플라빈-C(4a)-(하이드로)퍼옥사이드보다는 플라빈-N(5)-옥사이드의 사용을 포함한다.[2][3]
비산화환원반응
편집코리슴산 생성효소(CS)는 시킴산 경로의 마지막 단계인 코리슴산의 생성을 촉매한다. 코리슴산 생성효소에는 두 가지 부류가 있는데, 둘 다 FMN을 필요로 하지만, 환원제로써 NADPH를 필요로 하는 부류와 필요로 하지 않는 부류가 있다. 코리슴산 생성효소에 대해 제안된 메커니즘은 라디칼들을 포함한다. 라디칼 플라빈은 기질 유사체를 사용하지 않고, 분광학적으로 검출되지 않기 때문에 수명이 짧을 것으로 제안되었다. 그러나 플루오린화 기질을 사용시 중성 플라빈 세미퀴논이 검출되었다.[22]
복잡한 플라보효소
편집글루탐산 생성효소는 α-케토글루타르산을 L-글루탐산으로 전환시키는 반응을 촉매하며, L-글루타민은 이 반응의 질소원으로 작용한다. 모든 글루탐산 생성효소는 철-황 클러스터와 FMN을 함유하는 철-황 플라보단백질이다. 글루탐산 생성효소의 3가지 부류는 글루탐산 생성효소의 아미노산 서열 및 생화학적 특성에 따라 분류된다. 글루탐산 생성효소에는 3가지 부류가 있지만, 이들은 모두 동일한 메커니즘을 통해 작동한다고 믿어지는데, FMN을 먼저 환원시키는 것만 다를 뿐이다. 글루탐산 생성효소는 2개의 글루탐산 분자를 생성하는데, 1개는 글루타민의 가수분해(글루탐산과 암모니아를 생성함)에 의한 것이고, 다른 1개는 FMN에 의해 글루탐산으로 환원되는 α-케토글루타르산을 공격하는 첫 번째 반응에서 생성된 암모니아에 의한 것이다.[22]
임상적 중요성
편집플라보단백질 관련 질병
편집플라보단백질의 중요성으로 인해 사람의 플라보단백질의 약 60%가 돌연변이시 사람에게 질병을 일으킨다는 것은 그리 놀라운 일이 아니다.[16] 어떤 경우에는 FAD 또는 FMN에 대한 친화력이 감소하기 때문에 리보플라빈의 과다 섭취는 제2형 글루타르산혈증(다중 아실 조효소 A 탈수소효소 결핍증)과 같은 질병 증상을 완화시킬 수 있다.[9] 게다가 리보플라빈 결핍 그 자체(그리고 FAD와 FMN의 결핍으로 인해)는 건강 문제를 일으킬 수 있다.[9] 예를 들어, 근위축성 측색 경화증 환자에서 FAD 합성의 수준이 감소하였다.[9] 이러한 두 가지 경로 모두 발달 이상, 위장관 이상, 지방 분해 결합, 빈혈, 신경학적 문제, 암, 심혈관계 질환, 편두통, 시력 악화, 피부 병변의 악화를 포함한 다양한 증상들을 유발할 수 있다.[9] 따라서 제약 업계는 특정한 경우에 식단을 보충하기 위해 리보플라빈을 생산한다. 2008년에 리보플라빈에 대한 전세게 수요는 연간 6,000톤이었으며, 생산 능력은 10,000톤에 달했다.[4] 1억 5천만 달러~5억 달러 규모의 이 시장은 의료용 뿐만 아니라 농업에서 동물 사료 보충제 및 식품 착색제로 사용된다.[4]
의약품 설계
편집일반적인 항생제에 대한 세균의 항생제 내성이 증가함에 따라 새로운 항생제의 설계는 과학 연구에서 중요한 문제이다. FAD를 사용하는 특정 대사 단백질(석신산 탈수소효소)은 세균의 독성에 필수적이기 때문에 FAD 합성을 목표로 하거나 FAD 유사체를 만드는 것이 유용한 연구 분야가 될 수 있다.[25] 이미 과학자들은 FAD가 보통 한 번 묶인다고 가정하는 2개의 구조를 결정했는데, 분자가 본질적으로 반으로 접혀서 아데닌과 아이소알록사진 고리가 쌓이는 것을 야기하는 확장 입체구조와 나비형 입체 구조가 그것이다.[13] 유사한 방식으로 결합할 수 있지만 단백질 기능을 허용하지 않는 FAD 유사 모방 분자는 세균의 감염을 억제하는 유용한 메커니즘이 될 수 있다.[13] 또는 FAD 합성을 차단하는 약물이 동일한 목표를 달성할 수 있다. 이는 사람과 세균의 FAD 합성이 매우 다른 효소들에 의존하기 때문에 세균의 FAD 생성효소를 표적으로 하는 약물은 사람의 FAD 생성효소에 영향을 주지 않을 것이라는 것을 의미한다.[26]
광유전학
편집광유전학은 비침습적인 방법으로 생물학적 사건들을 조절할 수 있도록 한다.[27] 이 분야는 최근 몇 년간 청색광 이용 FAD 도메인(Blue-Light-Utilizing FAD domains, BLUF)과 같은 빛의 감도를 유발하는 도구를 포함하여 여러 가지 새로운 도구들을 활용해 발전했다. 청색광 이용 FAD 도메인은 식물과 세균의 광수용체로부터 유래한 100~140개의 아미노산 서열을 가지고 있다.[27] 다른 광수용체들과 마찬가지로, 빛은 청색광 이용 FAD 도메인의 구조적인 변화를 야기하여 다운스트림 상호작용을 방해한다.[27] 현재의 연구는 청색광 이용 FAD 도메인이 추가된 단백질들과 다른 외부 요인들이 단백질에 어떻게 영향을 미칠 수 있는지를 연구한다.[27]
치료 모니터링
편집신체에는 트립토판, 콜라겐, FAD, NADH, 포르피린을 비롯한 고유의 형광을 갖고 있는 많은 분자들이 있다.[28] 과학자들은 질병의 진행이나 치료 효과를 모니터링하거나 진단을 돕기 위해 이들 분자들을 이용한다. 예를 들어, FAD와 NADH의 고유 형광은 정상 조직과 침습성 구강암의 초기 징후인 구강 점막하 섬유증(oral submucous fibrosis)에서 다양하다.[28] 따라서 의사들은 표준 생검과는 달리 진단과 치료를 돕기 위해 형광을 사용해 왔다.[28]
추가 이미지들
편집-
FADH2
같이 보기
편집- 보조 인자
- 플라빈 모노뉴클레오타이드(FMN)
- 니코틴아마이드 아데닌 다이뉴클레오타이드(NAD)
- 니코틴아마이드 아데닌 다이뉴클레오타이드 인산(NADP)
각주
편집- ↑ Teufel, Robin; Agarwal, Vinayak; Moore, Bradley S. (2016년 4월 1일). “Unusual flavoenzyme catalysis in marine bacteria”. 《Current Opinion in Chemical Biology》 31: 31–39. doi:10.1016/j.cbpa.2016.01.001. ISSN 1879-0402. PMC 4870101. PMID 26803009.
- ↑ 가 나 Teufel, R; Miyanaga, A; Michaudel, Q; Stull, F; Louie, G; Noel, JP; Baran, PS; Palfey, B; Moore, BS (2013년 11월 28일). “Flavin-mediated dual oxidation controls an enzymatic Favorskii-type rearrangement.”. 《Nature》 503 (7477): 552–6. doi:10.1038/nature12643. PMC 3844076. PMID 24162851.
- ↑ 가 나 Teufel, Robin; Stull, Frederick; Meehan, Michael J.; Michaudel, Quentin; Dorrestein, Pieter C.; Palfey, Bruce; Moore, Bradley S. (2015년 7월 1일). “Biochemical Establishment and Characterization of EncM's Flavin-N5-oxide Cofactor”. 《Journal of the American Chemical Society》 137 (25): 8078–8085. doi:10.1021/jacs.5b03983. ISSN 1520-5126. PMC 4720136. PMID 26067765.
- ↑ 가 나 다 Abbas CA, Sibirny AA (Jun 2011). “Genetic control of biosynthesis and transport of riboflavin and flavin nucleotides and construction of robust biotechnological producers”. 《Microbiology and Molecular Biology Reviews》 75 (2): 321–60. doi:10.1128/mmbr.00030-10. PMC 3122625. PMID 21646432.
- ↑ Hayashi H (2013). 《B Vitamins and Folate: Chemistry, Analysis, Function and Effects》. Cambridge, UK: The Royal Society of Chemistry. 7쪽. ISBN 978-1-84973-369-4.
- ↑ Warburg O, Christian W (1938). “Isolation of the prosthetic group of the amino acid oxidase”. 《Biochemische Zeitschrift》 298: 150–168.
- ↑ Metzler DE, Metzler CM, Sauke DJ (2003). 《Biochemistry》 2판. San Diego: Harcourt, Academic Press. ISBN 978-0-12-492541-0.
- ↑ 가 나 Devlin TM (2011). 《Textbook of Biochemistry: with Clinical Correlations》 7판. Hoboken, NJ: John Wiley & Sons. ISBN 978-0-470-28173-4.
- ↑ 가 나 다 라 마 바 사 아 자 차 카 Barile M, Giancaspero TA, Brizio C, Panebianco C, Indiveri C, Galluccio M, Vergani L, Eberini I, Gianazza E (2013). “Biosynthesis of flavin cofactors in man: implications in health and disease”. 《Current Pharmaceutical Design》 19 (14): 2649–75. doi:10.2174/1381612811319140014. PMID 23116402.
- ↑ Teufel, Robin; Miyanaga, Akimasa; Michaudel, Quentin; Stull, Frederick; Louie, Gordon; Noel, Joseph P.; Baran, Phil S.; Palfey, Bruce; Moore, Bradley S. (2013년 11월 28일). “Flavin-mediated dual oxidation controls an enzymatic Favorskii-type rearrangement”. 《Nature》 503 (7477): 552–556. doi:10.1038/nature12643. ISSN 1476-4687. PMC 3844076. PMID 24162851.
- ↑ 가 나 다 라 마 바 Kim HJ, Winge DR (May 2013). “Emerging concepts in the flavinylation of succinate dehydrogenase”. 《Biochimica et Biophysica Acta》 1827 (5): 627–36. doi:10.1016/j.bbabio.2013.01.012. PMC 3626088. PMID 23380393.
- ↑ Lewis JA, Escalante-Semerena JC (Aug 2006). “The FAD-dependent tricarballylate dehydrogenase (TcuA) enzyme of Salmonella enterica converts tricarballylate into cis-aconitate”. 《Journal of Bacteriology》 188 (15): 5479–86. doi:10.1128/jb.00514-06. PMC 1540016. PMID 16855237.
- ↑ 가 나 다 Kuppuraj G, Kruise D, Yura K (Nov 2014). “Conformational behavior of flavin adenine dinucleotide: conserved stereochemistry in bound and free states”. 《The Journal of Physical Chemistry B》 118 (47): 13486–97. doi:10.1021/jp507629n. PMID 25389798.
- ↑ Monteira M (2013). 《B Vitamins and Folate: Chemistry, Analysis, Function and Effects》. Cambridge, UK: The Royal Society of Chemistry. 94쪽. ISBN 978-1-84973-369-4.
- ↑ 가 나 다 Macheroux P, Kappes B, Ealick SE (Aug 2011). “Flavogenomics--a genomic and structural view of flavin-dependent proteins”. 《The FEBS Journal》 278 (15): 2625–34. doi:10.1111/j.1742-4658.2011.08202.x. PMID 21635694.
- ↑ 가 나 다 라 Lienhart WD, Gudipati V, Macheroux P (Jul 2013). “The human flavoproteome”. 《Archives of Biochemistry and Biophysics》 535 (2): 150–62. doi:10.1016/j.abb.2013.02.015. PMC 3684772. PMID 23500531.
- ↑ Hühner J, Ingles-Prieto Á, Neusüß C, Lämmerhofer M, Janovjak H (Feb 2015). “Quantification of riboflavin, flavin mononucleotide, and flavin adenine dinucleotide in mammalian model cells by CE with LED-induced fluorescence detection”. 《Electrophoresis》 36 (4): 518–25. doi:10.1002/elps.201400451. PMID 25488801.
- ↑ Stryer L, Berg JM, Tymoczko JL (2007). 《Biochemistry》 6판. New York: Freeman. ISBN 978-0-7167-8724-2.
- ↑ 가 나 다 Mansoorabadi SO, Thibodeaux CJ, Liu HW (Aug 2007). “The diverse roles of flavin coenzymes--nature's most versatile thespians”. 《The Journal of Organic Chemistry》 72 (17): 6329–42. doi:10.1021/jo0703092. PMC 2519020. PMID 17580897.
- ↑ King MW. “Vitamins, Minerals, Supplements”. 《The Medical Biochemistry Page》.
- ↑ Garma, Leonardo D.; Medina, Milagros; Juffer, André H. (2016년 11월 1일). “Structure-based classification of FAD binding sites: A comparative study of structural alignment tools”. 《Proteins: Structure, Function, and Bioinformatics》 (영어) 84 (11): 1728–1747. doi:10.1002/prot.25158. ISSN 1097-0134. PMID 27580869.
- ↑ 가 나 다 라 마 바 사 아 자 Fagan RL, Palfey BA (2010). “Flavin-Dependent Enzymes”. 《Comprehensive Natural Products II Chemistry and Biology》 7: 37–113.
- ↑ 가 나 Hanukoglu I (2017). “Conservation of the Enzyme-Coenzyme Interfaces in FAD and NADP Binding Adrenodoxin Reductase-A Ubiquitous Enzyme”. 《Journal of Molecular Evolution》 85 (5): 205–218. doi:10.1007/s00239-017-9821-9. PMID 29177972.
- ↑ Hanukoglu I (1996). 《Electron transfer proteins of cytochrome P450 systems》 (PDF). 《Adv. Mol. Cell Biol.》. Advances in Molecular and Cell Biology 14. 29–55쪽. doi:10.1016/S1569-2558(08)60339-2. ISBN 9780762301133.
- ↑ McNeil MB, Fineran PC (May 2013). “Prokaryotic assembly factors for the attachment of flavin to complex II”. 《Biochimica et Biophysica Acta》 1827 (5): 637–47. doi:10.1016/j.bbabio.2012.09.003. PMID 22985599.
- ↑ Serrano A, Ferreira P, Martínez-Júlvez M, Medina M (2013). “The prokaryotic FAD synthetase family: a potential drug target”. 《Current Pharmaceutical Design》 19 (14): 2637–48. doi:10.2174/1381612811319140013. PMID 23116401.
- ↑ 가 나 다 라 Christie JM, Gawthorne J, Young G, Fraser NJ, Roe AJ (May 2012). “LOV to BLUF: flavoprotein contributions to the optogenetic toolkit”. 《Molecular Plant》 5 (3): 533–44. doi:10.1093/mp/sss020. PMID 22431563.
- ↑ 가 나 다 Sivabalan S, Vedeswari CP, Jayachandran S, Koteeswaran D, Pravda C, Aruna PR, Ganesan S (2010). “In vivo native fluorescence spectroscopy and nicotinamide adinine dinucleotide/flavin adenine dinucleotide reduction and oxidation states of oral submucous fibrosis for chemopreventive drug monitoring”. 《Journal of Biomedical Optics》 15 (1): 017010. doi:10.1117/1.3324771. PMID 20210484.
외부 링크
편집- FAD bound to proteins in the PDB
- FAD entry in the NIH Chemical Database